Questão 01 sobre Sais e Óxidos: (Fuvest) Molibdato de amônio é usado como fonte de molibdênio para o crescimento das plantas. Sabendo que este elemento, de símbolo Mo, pertence a mesma família do crômio, Cr, e que a fórmula do íon cromato é (CrO4)2-, a fórmula do molibdato de amônio é:
a) NH2MoO2.
b) NH3MoO3.
c) (NH3)2MoO4.
d) NH4MoO4.
e) (NH4)2MoO4.
Questão 02. (Fuvest) Hidroxiapatita, mineral presente em ossos e dentes, é constituída de íons fosfato (PO4)-3 e íons hidróxido.
A sua fórmula química pode ser representada por Cax(PO4)3(OH). O valor de x nesta fórmula é:
a) 1.
b) 2.
c) 3.
d) 4.
e) 5.
Questão 03. (Cesgranrio) O sonar, equipamento usado em submarinos para detectar a posição de objetos imersos em água, utiliza-se da emissão de ultrassom e da recepção e identificação do eco. Para tanto, ele é provido de uma pastilha de titanato de bário (BaTiO3), que pode ser obtido a partir da reação entre um óxido de titânio e o hidróxido de bário.
Identifique, nas opções adiante, o óxido usado na reação citada e a sua devida classificação.
a) TiO – básico.
b) Ti2O3 – anfótero.
c) TiO2 – peróxido.
d) TiO2 – anfótero.
e) TiO3 – ácido.
Questão 04 sobre Sais e Óxidos: (PUC) Considere as seguintes substâncias:
I. Cal virgem, CaO.
II. Cal hidratada, Ca (OH)2.
III. Gipsita, CaSO4, 2 H2O.
De acordo com as regras de nomenclatura de substâncias inorgânicas, os nomes desses compostos são, respectivamente:
a) peróxido de cálcio, hidreto de cálcio e sulfato de cálcio anidro.
b) monóxido de cálcio, hidróxido de cálcio e sulfeto hidratado de cálcio.
c) óxido de cálcio, hidreto de cálcio e sulfito de cálcio diidratado.
d) peróxido de cálcio, hidreto de cálcio e sulfato de cálcio hidratado.
e) óxido de cálcio, hidróxido de cálcio e sulfato de cálcio diidratado.
Questão 05. (Faap) Os elementos carbono e alumínio podem combinar-se com o oxigênio, originando os compostos:
Ca) 2O3, Al 2O3.
b) CO2, Al3O4.
c) CO, AlO.
d) CO2, Al2O3.
e) CO2, AlO.
Questão 06. (Unaerp) A figura a seguir mostra as substâncias existentes nas caixas e nos chamados “palitos de fósforo” e, de acordo com ela, constatamos que o fósforo é uma substância pertencente às caixas e não aos palitos. Assim, as substâncias existentes nos palitos são K2Cr2O7, Sb2S3 e outras.
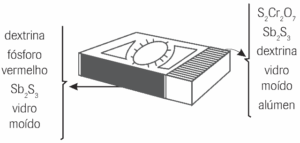
À substância K2Cr2O7 e aos elementos Sb e S, chamamos, respectivamente:
a) dicromato de sódio, antimônio e potássio.
b) permanganato de potássio, chumbo e sódio.
c) dicromato de potássio, chumbo e enxofre.
d) permanganato de potássio, antimônio e enxofre.
e) dicromato de potássio, antimônio e enxofre.
Questão 07 sobre Sais e Óxidos: (Mackenzie) Átomos neutros de um certo elemento representativo M apresentam dois elétrons em sua camada de valência.
As fórmulas corretas para seu óxido normal e brometo são, respectivamente:
a) M 2O e MBr.
b) MO2 e MBr2.
c) MO e MBr2.
d) M 2O2 e M2Br.
e) M2O e MBr2.
Questão 08. (FGV) Uma solução obtida pela adição de sulfato de alumínio e nitrato de amônio sólidos em água contém os íons NH+4(aq), Al3+(aq), SO42-(aq) e NO–3(aq).
As citadas substâncias podem ser representadas pelas fórmulas:
a) AlSO4 e (NH4)3NO3.
b) Al2SO4 e (NH4)3NO.
c) Al2(SO4)3 e NH4NO3.
d) Al3SO4 e NH4NO3.
e) Al3(SO4)2 e NH4(NO3)2.
Questão 09. (UFV) Cloreto de potássio, fosfato de cálcio, nitrato de sódio e sulfato de amônio são utilizados como fertilizantes na agricultura. As fórmulas correspondentes a estes sais são, respectivamente:
a) PC3, CaPO4, NaNO3, (NH4)2SO4.
b) KCl, Ca3(PO4)2, NaNO2, (NH4)2SO4.
c) KCl, Ca2(PO4)3, NaNO2, (NH4)2(SO4)3.
d) PCl3, Ca3(PO4)2, NaNO3, (NH4)2SO4.
e) KCl, Ca3(PO4)2, NaNO3, (NH4)2SO4.
Questão 10 sobre Sais e Óxidos: (UFRGS) No processo de produção do sal refinado, a lavagem do sal marinho provoca a perda do iodo natural, sendo necessário, depois, acrescentá-lo na forma de iodeto de potássio. Outra perda significativa é a de íons de magnésio, presentes no sal marinho na forma de cloreto de magnésio e sulfato de magnésio. Durante este processo são também adicionados alvejantes como o carbonato de sódio.
As fórmulas representativas das substâncias em negrito no texto anterior são, respectivamente:
a) KI, MgCl, MgSO4 e NaCO3.
b) K2I, MgCl2, Mg2SO4 e Na2CO3.
c) K2I, Mg2Cl, MgSO4 e Na(CO3)2.
d) KI, MgCl2, MgSO4 e Na2CO3.
e) KI2, Mg2Cl, Mg(SO4)2 e Na3CO3.
🔵 >>> Confira a lista completa com todos os exercícios de Química.
Gabarito com as respostas da lista de exercícios sobre Funções Inorgânicas: Sais e Óxidos:
01. E;
02. E;
03. D;
04. E;
05. D;
06. E;
07. C;
08. C;
09. E;
10. D
Doutorando em Genética e Biologia Molecular – UESC-BA
Mestre em Genética e Biologia Molecular – UESC-BA
Pós-Graduado em Metodologia do Ensino de Biologia e Química – FAEL
Licenciado em Ciências Biologias – IFMT/Campus Juína
