Questão 01 sobre Efeitos Coligativos: Unifor-CE – Para identificar três sais de sódio, contidos em frascos não rotulados, que podem ser o sulfato, o cloreto ou o fosfato, foram preparadas três soluções aquosas de concentração 0,5 mol do sal por kg de água, cada uma contendo apenas um desses sais.
Sob pressão constante, mediu-se a elevação, ∆T, da temperatura de ebulição dessas soluções encontrando-se os valores 0,50, 0,75 e 1,00ºC. A correspondência correta dos valores obtidos com o sal utilizado no preparo das soluções é:

Questão 02. FUVEST-SP – Numa mesma temperatura, foram medidas as pressões de vapor dos três sistemas ao abaixo.

Os resultados, para esses três sistemas, foram: 105,0, 106,4 e 108,2 mmHg, não necessariamente nessa ordem. Tais valores são, respectivamente, as pressões de vapor dos sistemas:

Questão 03 sobre Efeitos Coligativos: Unifor-CE – Quando se comparam soluções aquosas de mesma concentração, em mol/L, de cloreto de sódio e cloreto de potássio pode-se afirmar que possuem idênticas propriedades:
I. coligativas;
II. químicas;
III. físicas, à mesma temperatura.
Dessas afirmações somente:
a) I é correta.
b) II é correta.
c) III é correta.
d) I e II são corretas.
e) II e III são corretas.
Questão 04. UFPE – O gráfico abaixo representa a pressão de vapor (eixo das ordenadas), em atm, em função da temperatura (eixo das abcissas), em ºC, de três amostras, I, II e III.
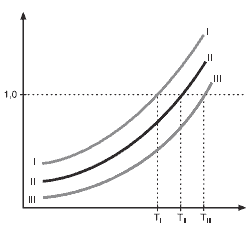
Se uma destas amostras for de água pura e as outras duas de água salgada, podemos afirmar que:
a) a amostra I é a amostra de água salgada;
b) a amostra I é a mais volátil;
c) a amostra II é mais concentrada que a amostra III;
d) a amostra I é a menos volátil;
e) na temperatura TIII e 1 atm a amostra II ainda não entrou em ebulição.
Questão 05. FATEC-SP – O gráfico a seguir mostra a variação da pressão de vapor de três diferentes substâncias — A, B e C — em função da temperatura.
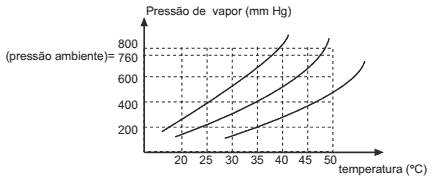
Analisando o gráfico, podemos concluir que:
a) B é mais volátil que A a 25 °C e a pressão ambiente.
b) C tem ponto de ebulição menor que B sob qualquer pressão.
c) se B for resfriado de 40 °C para 35 °C, a 400 mmHg, haverá condensação.
d) a 760 mmHg e 35 °C, B e C encontram-se em ebulição.
e) não há fase líquida de A a 30 °C e 400 mmHg.
Questão 06 sobre Efeitos Coligativos: Unifor-CE – Considere a tabela abaixo.
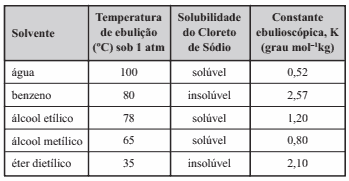
Dado:
lei de Raoult
∆T = K x molalidade
A um quilograma de cada um dos solventes acima adiciona-se 0,01 mol de cloreto de sódio. Sob pressão de 1 atm, aquece-se cada um desses sistemas. A maior elevação da temperatura de ebulição será observada no sistema cujo solvente é:
a) álcool etílico;
b) benzeno;
c) água;
d) álcool metílico;
e) éter dietílico.
🔵 >>> Confira a lista completa com todos os exercícios de Química.
Gabarito com as respostas dos exercícios de Química sobre Efeitos Coligativos:
01. b;
02. c;
03. a;
04. a;
05. e;
06. c;
Doutorando em Genética e Biologia Molecular – UESC-BA
Mestre em Genética e Biologia Molecular – UESC-BA
Pós-Graduado em Metodologia do Ensino de Biologia e Química – FAEL
Licenciado em Ciências Biologias – IFMT/Campus Juína
