Questão 01 sobre Calorimetria: (Uerj) Em um laboratório, as amostras X e Y, compostas do mesmo material, foram aquecidas a partir da mesma temperatura inicial até determinada temperatura final. Durante o processo de aquecimento, a amostra X absorveu uma quantidade de calor maior que a amostra Y. Considerando essas amostras, as relações entre os calores específicos cX e cY, as capacidades térmicas CX e CY e as massas m X e mY são descritas por:
a) cX = cY CX > CY mX > mY
b) cX > cY CX = CY mX = mY
c) cX = cY CX > CY mX = mY
d) cX > cY CX = CY mX > mY
Questão 02 sobre Calorimetria: (PUC-RJ) Três cubos de gelo de 10,0 g, todos eles a 0,0 °C, são colocados dentro de um copo vazio e expostos ao sol até derreterem completamente, ainda a 0,0°C. Calcule a quantidade total de calor requerida para isto ocorrer, em calorias. Considere o calor latente de fusão do gelo LF = 80 cal/g:
a) 3,7 10-1
b) 2,7 101
c) 1,1 102
d) 8,0 102
e) 2,4 103
Questão 03. (Ufpr) O gráfico abaixo, obtido experimentalmente, mostra a curva de aquecimento que relaciona a temperatura de uma certa massa de um líquido em função da quantidade de calor a ele fornecido.
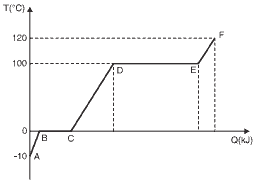
Sabemos que, por meio de gráficos desse tipo, é possível obter os valores do calor específico e do calor latente das substâncias estudadas. Assinale a alternativa que fornece corretamente o intervalo em que se pode obter o valor do calor latente de vaporização desse líquido.
a) AB.
b) BD.
c) DE.
d) CD.
e) EF.
Questão 04 sobre Calorimetria: (Unesp) A liofilização é um processo de desidratação de alimentos que, além de evitar que seus nutrientes saiam junto com a água, diminui bastante sua massa e seu volume, facilitando o armazenamento e o transporte. Alimentos liofilizados também têm seus prazos de validade aumentados, sem perder características como aroma e sabor.

O processo de liofilização segue as seguintes etapas:
I. O alimento é resfriado até temperaturas abaixo de 0°C, para que a água contida nele seja solidificada.
II. Em câmaras especiais, sob baixíssima pressão (menores do que 0,006 atm), a temperatura do alimento é elevada, fazendo com que a água sólida seja sublimada. Dessa forma, a água sai do alimento sem romper suas estruturas moleculares, evitando perdas de proteínas e vitaminas.
O gráfico mostra parte do diagrama de fases da água e cinco processos de mudança de fase, representados pelas setas numeradas de 1 a 5.
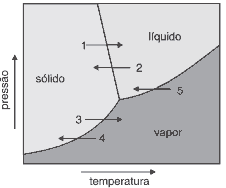
A alternativa que melhor representa as etapas do processo de liofilização, na ordem descrita, é:
a) 4 e 1.
b) 2 e 1.
c) 2 e 3.
d) 1 e 3.
e) 5 e 3.
Questão 05 sobre Calorimetria: (Ufpa) A presença de vapor d’água num ambiente tem um papel preponderante na definição do clima local. Uma vez que uma quantidade de água vira vapor, absorvendo uma grande quantidade de energia, quando esta água se condensa libera esta energia para o meio ambiente. Para se ter uma ideia desta quantidade de energia, considere que o calor liberado por 100 g de água no processo de condensação seja usado para aquecer uma certa massa m de água líquida de 0°C até 100°C.
(Dados: Calor latente de fusão do gelo LF = 80 cal/g; Calor latente de vaporização LV = 540 cal/g; Calor específico da água, c = 1 cal/g°C.)
Com base nas informações apresentadas, calcula-se que a massa m, de água aquecida, é:
a) 540 g
b) 300 g
c) 100 g
d) 80 g
e) 6,7 g
Questão 06. (Uepg) O gráfico abaixo mostra a evolução da temperatura de um corpo de massa m, constituído por uma substância pura, em função da quantidade de calor que lhe é fornecida. Com base nas informações desse gráfico, assinale o que for correto.
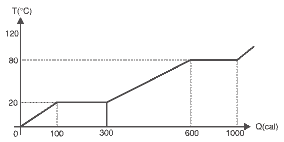
01) Em T = 20°C e T = 80°C o corpo sofre mudanças de fases.
02) A quantidade de calor cedido ao corpo enquanto a sua temperatura variou entre 20°C e 80°C é denominado calor sensível.
04) Em T = 0°C o corpo se encontra na fase sólida.
08) O calor cedido ao corpo durante as mudanças de fase é denominado calor latente.
Questão 07 sobre Calorimetria: (Uel) O homem utiliza o fogo para moldar os mais diversos utensílios. Por exemplo, um forno é essencial para o trabalho do ferreiro na confecção de ferraduras. Para isso, o ferro é aquecido até que se torne moldável. Considerando que a massa de ferro empregada na confecção de uma ferradura é de 0,5 kg, que a temperatura em que o ferro se torna moldável é de 520°C e que o calor específico do ferro vale 0,1 cal/g°C, assinale a alternativa que fornece a quantidade de calor, em calorias, a ser cedida a essa massa de ferro para que possa ser trabalhada pelo ferreiro.
Dado: temperatura inicial da ferradura: 20°C.
a) 25
b) 250
c) 2500
d) 25000
e) 250000
Questão 08. (Ufrgs) O gráfico a seguir representa o calor absorvido por unidade de massa, Q/m, em função das variações de temperatura DT para as substâncias ar, água e álcool, que recebem calor em processos em que a pressão é mantida constante.
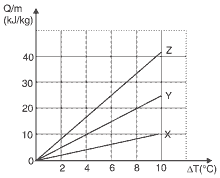
(Considere que os valores de calor específico do ar, do álcool e da água são, respectivamente, 1,0 kJ/kg.°C, 2,5 kJ/kg.°C e 4,2 kJ/kg.°C.)
Com base nesses dados, é correto afirmar que as linhas do gráfico identificadas pelas letras X, Y e Z, representam, respectivamente,
a) o ar, o álcool e a água.
b) o ar, a água e o álcool.
c) a água, o ar e o álcool.
d) a água, o álcool e o ar.
e) o álcool, a água e o ar.
Questão 09. (Fuvest) Em um recipiente termicamente isolado e mantido a pressão constante, são colocados 138 g de etanol líquido. A seguir, o etanol é aquecido e sua temperatura T é medida como função da quantidade de calor Q a ele transferida. A partir do gráfico de TxQ, apresentado na figura abaixo, pode-se determinar o calor específico molar para o estado líquido e o calor latente molar de vaporização do etanol como sendo, respectivamente, próximos de:
Dados: Fórmula do etanol = C
2H5OH; Massas molares =
C(12g/mol), H(1g/mol), O(16g/mol).
a) 0,12 kJ/(mol°C) e 36 kJ/mol.
b) 0,12 kJ/(mol°C) e 48 kJ/mol.
c) 0,21 kJ/(mol°C) e 36 kJ/mol.
d) 0,21 kJ/(mol°C) e 48 kJ/mol.
e) 0,35 kJ/(mol°C) e 110 kJ/mol.
Questão 10 sobre Calorimetria: (Fatec) No anúncio promocional de um ferro de passar roupas a vapor, é explicado que, em funcionamento, o aparelho borrifa constantemente 20 g de vapor de água a cada minuto, o que torna mais fácil o ato de passar roupas. Além dessa explicação, o anúncio informa que a potência do aparelho é de 1 440 W e que sua tensão de funcionamento é de 110 V. Da energia utilizada pelo ferro de passar roupas, uma parte é empregada na transformação constante de água líquida em vapor de água. A potência dissipada pelo ferro para essa finalidade é, em watts, Adote:
• temperatura inicial da água: 25°C
• temperatura de mudança da fase líquida para o vapor: 100°C
• temperatura do vapor de água obtido: 100°C
• calor específico da água: 1 cal/(g°C)
• calor latente de vaporização da água: 540 cal/g
• 1 cal = 4,2 J
a) 861.
b) 463.
c) 205.
d) 180.
e) 105.
🔵 >>> Verifique todos os nossos exercícios e atividades de Física.
Gabarito com as resposta da lista com 10 Exercícios de física sobre Calorimetria:
01. a;
02. e;
03. c;
04. c;
05. a;
06. 01 + 02 + 04 + 08 = 15;
07. a;
08. a;
09. a;
10. a
Doutorando em Genética e Biologia Molecular – UESC-BA
Mestre em Genética e Biologia Molecular – UESC-BA
Pós-Graduado em Metodologia do Ensino de Biologia e Química – FAEL
Licenciado em Ciências Biologias – IFMT/Campus Juína
