Questão 01 sobre Óxidos: (Fgv SP/1996). Das substâncias abaixo, podemos classificar como óxidos ácidos:
01. SO2 e Mn2O7
02. CO2 e CO
03. CO2 e N2O
04. P2O2 e ZnO
05. SiO2 e CO
Questão 02. (ITA SP/1997) Considere as afirmações sobre os óxidos de nitrogênio NO, N2O e NO2.
I. A formação destes óxidos, a partir de N2 e O2, é endotérmica.
II. Os números de oxidação dos átomos de nitrogênio nos óxidos NO, N2O e NO2 são, respectivamente, +2, +1, e +4.
III. O N2O é chamado de gás hilariante.
IV. O NO é o anidrido do ácido nítrico.
V. O NO2 é um gás colorido.
Estão CORRETAS:
a) Apenas II e IV.
b) Apenas III e V.
c) Apenas I, II, III e V.
d) Apenas I, II, IV e V.
e) Todas.
Questão 03 sobre Óxidos: (Udesc SC/2005) O gás SO2 é um dos principais poluentes atmosféricos, sendo que sua presença na atmosfera resulta em danos à saúde dos seres vivos. Esse gás é solúvel em água, podendo ser incorporado às gotículas de água que formam as nuvens, formando a substância H2SO3. Essa substância pode ainda reagir com H2O2 na atmosfera, para formar ácido sulfúrico. Esse é um dos caminhos para a formação da “chuva ácida”, sendo que a quantificação do ácido pode ser realizada pela reação com KOH, que gera K2SO4 e água.
As funções químicas relacionadas às substâncias de fórmula SO2, H2SO3, H2O2, KOH e K2SO4 são, respectivamente:
a) base, ácido, peróxido, óxido e sal.
b) sal, peróxido, base, ácido e óxido.
c) peróxido, ácido, ácido, base e sal.
d) óxido, ácido, peróxido, base e sal.
e) óxido, sal, base, ácido e sal.
Questão 04. (ITA SP/1996) Discutindo problemas relacionados com a obtenção de metais, alunos fizeram as afirmações listadas nas opções a seguir. Qual é a opção que contém a afirmação ERRADA?
a) As reservas minerais de ferro são muitíssimo maiores que as de cobre.
b) A redução de um mol de óxido de alumínio (Al2O3) exige muito mais energia que a redução de um mol de óxido de ferro (Fe2O3).
c) Sódio metálico foi obtido pela primeira vez por H. Davy através da eletrólise de NaOH fundido.
d) Alumínio metálico é obtido por redução de (Al2O3) em altos-fornos análogos aos utilizados no preparo de ferro metálico.
e) Embora o titânio seja relativamente abundante na crosta terrestre, jazidas de vulto desta substância são raras.
Questão 05 sobre Óxidos: (Puc SP/2001) O ponto de fusão de compostos iônicos está relacionado com a força de atração entre os íons no retículo (energia reticular). A lei de Coulomb é uma boa aproximação para determinar essa força de atração:
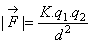
onde K é uma constante, q1 é a carga do cátion, q2 é a carga do ânion e d é a soma dos raios iônicos (d = rcátion + rânion ).
Considerando a lei de Coulomb e as propriedades periódicas, assinale a alternativa que apresenta os pontos de fusão (P.F.) dos compostos iônicos NaF, NaCl, MgO e NaBr em ordem crescente de temperatura.
a) P.F. NaCl < P.F. MgO < P.F. NaF < < P.F. NaBr
b) P.F. NaBr < P.F. NaCl < P.F. NaF < < P.F. MgO
c) P.F. MgO < P.F. NaBr < P.F. NaCl < < P.F. NaF
d) P.F. NaF < P.F. NaCl < P.F. NaBr < < P.F. MgO
e) P.F. NaBr < P.F. MgO < P.F. NaCl < < P.F. NaF
Questão 06. (Fuvest SP/2004/1ªFase) “São animadores os números da safra de grãos do Brasil, que deverá colher neste ano o recorde histórico de 120 milhões de toneladas. Com isto, o Brasil deverá tornar-se o maior exportador mundial de soja, suplantando os Estados Unidos”.
Folha de São Paulo, 2003
O acréscimo de produção de soja citado acarretará:
I. aumento do “buraco na camada de ozônio”, pois nas plantações de soja são utilizados clorofluorocarbonetos como fertilizantes.
II. maior consumo de água, necessária à irrigação, que, em parte, será absorvida pelo vegetal.
III. aumento da quantidade de CO2 atmosférico, diretamente produzido pela fotossíntese.
IV. aumento da área de solos ácidos, gerados pela calagem, em que se utiliza calcário com altos teores de óxido de cálcio e óxido de magnésio.
Dessas afirmações,
a) somente I é correta.
b) somente II é correta.
c) somente II e III são corretas.
d) somente III e IV são corretas.
e) todas são corretas.
Questão 07 sobre Óxidos: (ITA SP/1995) Considere as seguintes afirmações:
I. Óxidos como Na2O , MgO e ZnO são compostos iônicos.
II. Óxidos como K2O, BaO e CuO são básicos.
III. Óxidos de carbono, nitrogênio e enxofre são compostos moleculares.
IV. PbO2 e MnO2 são oxidantes fortes.
Destas afirmações estão CORRETAS:
a) Apenas I e II.
b) Apenas I e III.
c) Apenas III e IV.
d) Apenas I, II e III.
e) Todas.
Questão 08. (ITA SP/1994) Qual das opções abaixo contém a afirmação FALSA?
a) CrO3 é um óxido menos ácido do que o Cr2O3.
b) Para obter HCl gasoso basta juntar H2SO4 a sal de cozinha à frio.
c) Vidros para garrafas e janelas são obtidos fundindo juntos sílica, cal e soda.
d) Chama-se de superfosfato um adubo obtido pela interação de H2SO4 com trifosfato de cálcio.
e) Enquanto os óxidos dos metais alcalinos e dos metais alcalinos terrosos pulverizados costumam ser brancos, os óxidos dos metais de transição são, via de regra, fortemente coloridos.
Questão 09. (Ufse SE/1998) Carbono, alumínio, e lítio podem combinar-se com o oxigênio dando origem aos compostos:
a) C2O5, Al2O3, LiO
b) CO, AlO, LiO
c) CO2, AlO, Li2O3
d) CO2, Al2O3, Li2O
e) CO2, Al3O4, Li3O2
Questão 10 sobre Óxidos: (Unifor CE) Óxido de sódio e sulfeto de hidrogênio são substâncias formadas através de ligações, respectivamente:
a) iônica e covalente polar
b) covalente polar e iônica
c) iônica e iônica
d) covalente apolar e iônica
e) iônica e covalente apolar
🔵 >>> Confira a lista completa com todos os exercícios de Química.
Gabarito com as respostas dos exercícios de Química sobre Funções Químicas – Óxidos:
01. 01;
02. C;
RESOLUÇÃO
I- Verdadeiro
DHof NO = +90,4 kj/mol
DHof N2O = +81,56kj/mol
DHof NO2 = +33,85 kj/mol
II- Verdadeiro
NO………………NOX N=+2
N2O……………..NOX N=+1
NO2……………..NOX N=+4
III– Verdadeiro. Podendo também ser chamado de óxido nitroso ou protóxido de azoto.
IV- Falso. O anidrido do ácido nítrico é o N2O5. O NO é chamado de óxido nítrico.
V- Verdadeiro. Trata-se de um gás amarelo-acastanhado, altamente tóxico e com cheiro sufocante; é uma molécula diamagnética e é encontrada no nevoeiro fotoquímico.
03. D;
04. E;
RESOLUÇÃO
a- Verdadeiro.
Fe = 8,9% das reservas mundiais
Cu = 0,5% das reservas mundiais
b- Verdadeiro.
A produção de 1kg de alumínio consome 15 vezes mais energia que a produção de 1kg de aço.
c- Verdadeiro.
Em 1807 por H. Davy.
d- Verdadeiro.
Fornos especiais chamados de processo Hall.
e- Falso.
O elemento titânico aparece em 9º lugar em termos de porcentagem em massa.elemento % em massa oxigênio 46,5 silício 28 alumínio 8,3 ferro 5,6 cálcio 4,2 sódio 2,4 magnésio 2,3 potássio 2,1 titânio 0,6 hidrogênio 0,14
05. B;
06. B;
07. E;
RESOLUÇÃO
I- Verdadeiro, pois são óxidos metálicos
II- Verdadeiro, pois são óxidos metálicos com baixo NOX
III- Verdadeiro, pois são óxidos não-metálicos
IV- Verdadeiro, pois provoca fortes oxidações
08. A;
09. D;
10. A
Doutorando em Genética e Biologia Molecular – UESC-BA
Mestre em Genética e Biologia Molecular – UESC-BA
Pós-Graduado em Metodologia do Ensino de Biologia e Química – FAEL
Licenciado em Ciências Biologias – IFMT/Campus Juína
