Questão 01 sobre Estrutura do Átomo: (Unesp/2015) Uma das substâncias aglutinadoras que pode ser utilizada para nucleação artificial de nuvens é o sal iodeto de prata, de fórmula AgI. Utilizando os dados fornecidos na Classificação Periódica dos Elementos, é correto afirmar que o cátion e o ânion do iodeto de prata possuem, respectivamente:
a) 46 elétrons e 54 elétrons.
b) 48 elétrons e 53 prótons.
c) 46 elétrons e 54 elétrons.
d) 47 elétrons e 53 elétrons.
e) 47 prótons e 52 elétrons.
Questão 02. (Uece 2015) Há cerca de dois mil e quinhentos anos, o filósofo grego Demócrito disse que se dividirmos a matéria em pedacinhos, cada vez menores, chegaremos a grãozinhos indivisíveis, que são os átomos (a = não e tomo = parte). Em 1897, o físico inglês Joseph Thompson (1856-1940) descobriu que os átomos eram divisíveis: lá dentro havia o elétron, partícula com carga elétrica negativa. Em 1911, o neozelandês Ernest Rutherford (1871-1937) mostrou que os átomos tinham uma região central compacta chamada núcleo e que lá dentro encontravam-se os prótons, partículas com carga positiva.
Atente à figura a seguir, que representa o núcleo e a eletrosfera do átomo.
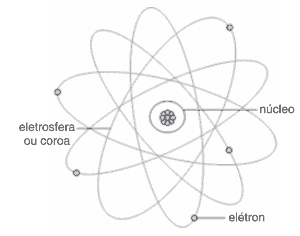
Com relação à figura acima, é correto afirmar que:
a) o núcleo é muito pequeno, por isso, tem pouca massa se comparado à massa do átomo.
b) mais de de toda a massa do átomo está na eletrosfera.
c) considerando as reais grandezas do núcleo e da eletrosfera do átomo, se comparadas às suas representações na figura, o tamanho da eletrosfera está desproporcional ao tamanho do núcleo.
d) a massa do núcleo é bem maior do que a massa da eletrosfera, cuja relação fica em torno de 100 vezes.
Questão 03 sobre Estrutura do Átomo: (Uem 2015) Sobre os principais fundamentos da teoria atômica de Dalton, assinale a(s) alternativa(s) correta(s).
01) A massa fixa de um elemento pode combinar-se com massas múltiplas de outro elemento para formar substâncias diferentes.
02) O átomo é semelhante a uma massa gelatinosa carregada positivamente, tendo cargas negativas espalhadas nessa massa.
04) A carga positiva de um átomo não está distribuída por todo o átomo, mas concentrada na região central.
08) Existem vários tipos de átomos e cada um constitui um elemento químico. Átomos de um mesmo elemento químico são idênticos, particularmente em seu peso.
16) Toda matéria é composta por átomos, que são partículas indivisíveis e não podem ser criados ou destruídos.
Questão 04. (Fgv 2015) O Brasil inaugurou em 2014 o Projeto Sirius, um acelerador de partículas que permitirá o desenvolvimento de pesquisa na área de materiais, física, química e biologia. Seu funcionamento se dará pelo fornecimento de energia a feixes de partículas subatômicas eletricamente carregadas: prótons e elétrons.
(http://www.brasil.gov.br/ciencia-e-tecnologia/2014/02/. Adaptado)
Na tabela, são apresentadas informações das quantidades de algumas partículas subatômicas para os íons X2- e A2+:
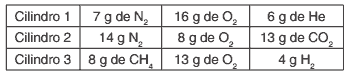
Nessa tabela, o nome do elemento X e o valor de y são, respectivamente:
a) argônio e 16.
b) argônio e 20.
c) enxofre e 16.
d) enxofre e 18.
e) enxofre e 20.
Questão 05 sobre Estrutura do Átomo: (Unesp/2014) Água coletada em Fukushima em 2013 revela radioatividade recorde
A empresa responsável pela operação da usina nuclear de Fukushima, Tokyo Electric Power (Tepco), informou que as amostras de água coletadas na central em julho de 2013 continham um nível recorde de radioatividade, cinco vezes maior que o detectado originalmente. A Tepco explicou que uma nova medição revelou que o líquido, coletado de um poço de observação entre os reatores 1 e 2 da fábrica, continha nível recorde do isótopo radioativo estrôncio-90.
(www.folha.uol.com.br. Adaptado.)
O estrôncio-90:

é o principal isótopo desse elemento químico encontrado nos reatores nucleares. Sobre esse isótopo, é correto afirmar que seu cátion bivalente possui
a) 38 prótons, 50 nêutrons e 36 elétrons.
b) 36 prótons, 52 nêutrons e 38 elétrons.
c) 38 prótons, 50 nêutrons e 38 elétrons.
d) 38 prótons, 52 nêutrons e 36 elétrons.
e) 36 prótons, 52 nêutrons e 36 elétrons.
Questão 06. (PUC-Rio) Um íon X-1 tem 18 elétrons e 20 nêutrons. Portanto, o elemento X tem:
a) número atômico 17.
b) 18 prótons.
c) 19 elétrons.
d) 19 nêutrons.
e) número de massa 38.
Questão 07 sobre Estrutura do Átomo: (G1 – cftmg/2014) Trata-se de um modelo no qual os átomos de um mesmo elemento químico possuem propriedades iguais. A união desses átomos na formação de compostos ocorre em proporções numéricas fixas e a reação química dos mesmos envolve apenas combinação, separação e rearranjo. Essa descrição refere-se ao modelo atômico de:
a) Bohr.
b) Dalton.
c) Thomson.
d) Rutherford.
Questão 08. (PUC-RS) O átomo, na visão de Thomson, é constituído de
a) níveis e subníveis de energia.
b) cargas positivas e negativas.
c) núcleo e eletrosfera.
d) grandes espaços vazios.
e) orbitais.
Questão 09. (Ufsj) Se um dado átomo possui 6 elétrons, 6 prótons e 7 nêutrons, é CORRETO afirmar que:
a) seu número atômico é 7.
b) há 13 partículas no núcleo.
c) ele está positivamente carregado.
d) seu número de massa é 12.
Questão 10 sobre Estrutura do Átomo: (Ufrgs) Na reunião da IUPAC, que celebrou o fim do Ano Internacional da Química, os mais novos elementos foram oficialmente denominados de fleróvio, em homenagem ao físico russo Georgiy Flerov, e de livermório, em homenagem ao Laboratório Livermore da Califórnia. Esses são os dois elementos mais pesados da tabela periódica e são altamente radioativos. O fleróvio (FL) apresenta número atômico 114 e número de massa 289, e o livermório (Lv) apresenta número atômico 116 e número de massa 292.
O número de nêutrons em cada átomo do elemento fleróvio e o número de nêutrons em cada átomo do elemento livermório são, respectivamente:
a) 114 e 116.
b) 175 e 176.
c) 189 e 192.
d) 289 e 292.
e) 403 e 408.
🔵 >>> Confira a lista completa com todos os exercícios de Química.
Gabarito com as respostas da lista de atividades de química sobre Estrutura do Átomo:
01. a;
02. c;
03. 01 + 08 + 16;
04. e;
05. d;
06. a;
07. b;
08. b;
09. b;
10. b
Doutorando em Genética e Biologia Molecular – UESC-BA
Mestre em Genética e Biologia Molecular – UESC-BA
Pós-Graduado em Metodologia do Ensino de Biologia e Química – FAEL
Licenciado em Ciências Biologias – IFMT/Campus Juína
