Questão 01 sobre Ácidos de Arrhenius: (UNIFESP) Para distinguir uma solução aquosa de HF (ácido fraco) de outra de HCl (ácido forte), de mesma concentração, foram efetuados os seguintes procedimentos independentes com cada uma das soluções:
I. Determinação da temperatura de congelamento do solvente.
II. Medida de pH.
III. Teste com uma tira de papel tornassol azul.
IV. Medida de condutibilidade elétrica das soluções.
Os procedimentos que permitem distinguir entre essas soluções são:
A) I, II e IV, apenas.
B) II, III e IV, apenas.
C) II e IV, apenas.
D) III e IV, apenas.
E) IV, apenas.
Questão 02. (UNA-MG) O nome dos ácidos apresentados a seguir são, respectivamente, H2SO3 HClO4 H2S H3PO4:
A) sulfuroso, perclórico, sulfídrico e fosfórico.
B) sulfídrico, clórico, sulfúrico e fosforoso.
C) sulfúrico, clorídrico, sulfuroso e ortofosfórico.
D) sulfuroso, clórico, sulfídrico e metafosforoso.
Questão 03 sobre Ácidos de Arrhenius: (UFU-MG–2008) Correlacione os ácidos da 1ª Coluna com as respectivas características e aplicações listadas na 2ª Coluna.
1ª COLUNA
I. H2SO4
II. H3PO4
III. HCl
IV. CH3COOH
V. HCN
2ª COLUNA
( ) Encontrado no comércio como ácido muriático.
( ) Usado para temperar saladas.
( ) Adicionado em bebidas e refrigerantes.
( ) Adicionado em baterias de automóveis.
( ) Extremamente tóxico.
Marque a alternativa que apresenta a sequência CORRETA de cima para baixo.
A) I, II, IV, V, III
B) III, IV, II, I, V
C) IV, II, III, V, I
D) IV, II, I, III, IV
Questão 04. (Mackenzie-SP–2007) O gambá, ao sentir-se acuado, libera uma mistura de substâncias de odor desagradável, entre elas o gás sulfídrico. Sobre esse gás, é INCORRETO afirmar que Dados:
Número atômico: H = 1; S = 16.
Massa molar (g.mol–1): H = 1; S = 32.
A) possui fórmula molecular HS.
B) ![]() é sua fórmula estrutural.
é sua fórmula estrutural.
C) em água, produz uma solução ácida.
D) apresenta cheiro de ovo podre.
E) tem massa molar igual a 34 g.mol–1.
Questão 05 sobre Ácidos de Arrhenius: (PUC Minas–2007) O dióxido de carbono presente na atmosfera se dissolve na água de chuva, originando ácido carbônico.O equilíbrio que representa CORRETAMENTE esse fenômeno é:
A) H2CO3(aq) CO(g) + H2O(l).
B) H2CO3(aq) CO(g) + H2O2(l).
C) H2CO3(aq) CO2(g) + H2O2(l).
D) H2CO3(aq) CO2(g) + H2O(l).
Questão 06. (UEPB) Observe o esquema a seguir:
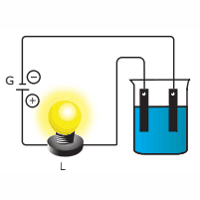
A força de um ácido é medida pelo seu grau de ionização (a), ou seja, pela relação entre o número de moléculas ionizadas e o número total de moléculas dissolvidas. Em qual das soluções – de mesma concentração e à mesma temperatura – a lâmpada (L) do esquema apresenta maior brilho?
A) HF
B) HNO3
C) H3PO4
D) H2S
E) H4SiO4
Questão 07 sobre Ácidos de Arrhenius: (UFC–2007) A força dos ácidos varia em função de uma série de propriedades, tais como: constituintes químicos, geometria da molécula, estado de oxidação das espécies envolvidas, etc.
Considerando os ácidos HClO, HBrO e HIO, é CORRETO afirmar que:
A) o HClO é um ácido mais fraco do que o HIO.
B) o HBrO é um ácido mais forte do que o HClO.
C) a ordem crescente de acidez é HIO, HBrO, HClO.
D) a ordem decrescente de acidez é HIO, HClO, HBrO.
E) os estados de oxidação do Cl, Br e I são –1, –2 e –3, respectivamente.
Questão 08. (FGV-SP–2008) Na tabela, são dadas as energias de ligação (kJ/mol) a 25 ºC para algumas ligações simples, para moléculas diatômicas entre H e os halogênios (X).
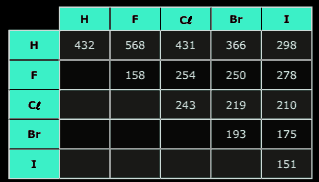
Analise as afirmações seguintes:
I. Entre os compostos HX, o HF é o ácido mais fraco e a sua ligação H—X é a mais forte.
II. A distância de ligação entre os átomos, nas moléculas X2, é maior no I2, já que a sua energia de ligação é a mais fraca.
III. A molécula com maior momento dipolar é o HI.
Está CORRETO o contido em:
A) I, II e III.
B) I e II, apenas.
C) I e III, apenas.
D) II e III, apenas.
E) II, apenas.
Questão 09. (ACAFE-SC) Os nomes dos ácidos oxigenados a seguir são, respectivamente, HNO2 HClO3 H2SO4 H2SO3 H3PO4:
A) nitroso, clórico, sulfúrico, sulfuroso e fosfórico.
B) nítrico, clorídrico, sulfuroso, sulfúrico e fosfórico.
C) nítrico, hipocloroso, sulfúrico, sulfuroso e fosforoso.
D) nitroso, perclórico, sulfuroso, sulfúrico e fosfórico.
E) nítrico, cloroso, sulfuroso, sulfúrico e hipofosforoso.
Questão 10 sobre Ácidos de Arrhenius: (UFC) Associe a coluna da esquerda com a da direita e assinale a alternativa CORRETA, de cima para baixo.
I. HClO4 ( ) Ácido hipocloroso
II. HClO2 ( ) Ácido clórico
III. HClO ( ) Ácido perclórico
IV. HClO3 ( ) Ácido cloroso
A) I, II, IV, III
B) II, III, I, IV
C) II, I, IV, III
D) III, IV, I, II
E) N.d.a
🔵 >>> Confira a lista completa com todos os exercícios de Química.
Gabarito com as respostas da lista de exercícios de Química sobre Ácidos de Arrhenius:
01. A;
02. A;
03. B;
04. A;
05. D;
06. B;
07. C;
08. B;
09. A;
10. D
Doutorando em Genética e Biologia Molecular – UESC-BA
Mestre em Genética e Biologia Molecular – UESC-BA
Pós-Graduado em Metodologia do Ensino de Biologia e Química – FAEL
Licenciado em Ciências Biologias – IFMT/Campus Juína
