Questão 01 sobre Interações Intermoleculares: (PUC Minas) Assinale o tipo predominante de interações entre as moléculas do éter dimetílico.
A) Interações do tipo dipolo permanente / carga.
B) Interações do tipo dipolo induzido / dipolo induzido.
C) Interações do tipo dipolo permanente / dipolo permanente.
D) Interações do tipo dipolo / ligação de hidrogênio.
Questão 02. (UEPG–PR) O nitrogênio, principal constituinte do ar atmosférico, é uma substância apolar que pode ser liquefeita a baixas temperaturas. Nesse estado, as forças que unem as moléculas umas às outras são conhecidas como:
A) ligações de hidrogênio.
B) interações dipolo-dipolo.
C) ligações metálicas.
D) pontes bissulfeto.
E) forças de London.
Questão 03 sobre Interações Intermoleculares: (UFMG) A estrutura I representa a vanilina, molécula responsável pelo aroma da baunilha, e as estruturas II, III e IV representam três de seus isômeros:
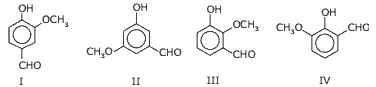
Todas essas moléculas podem formar ligações de hidrogênio entre grupos pertencentes à mesma molécula, EXCETO:
A) I.
B) II.
C) III.
D) IV.
Questão 04. (UFC) A atividade contraceptiva dos DIUs (Diafragmas Intrauterinos) modernos é atribuída, em partes, à ação espermicida de sais de cobre (II) que são gradativamente liberados por esses diafragmas no útero feminino. Quanto aos sais de cobre (II) em meio aquoso, assinale a alternativa CORRETA:
A) Apresentam interações íon-dipolo.
B) Permanecem no estado sólido.
C) Envolvem interações entre espécies apolares.
D) A configuração eletrônica do íon cobre (II) é [Ar] 3d8.
E) O íon cobre (II) encontra-se na forma reduzida, Cu2–.
Questão 05 sobre Interações Intermoleculares: (UFMG) Considere separadamente as substâncias tetracloreto de carbono, água, n-hexano e acetona, listadas na tabela de interações intermoleculares, nessa ordem.
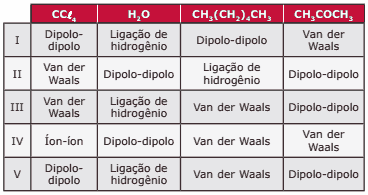
Questão 06. (UFC) Recentemente, uma pesquisa publicada na revista Nature (v. 405, p. 681, 2000) mostrou que a habilidade das lagartixas (víboras) em escalar superfícies lisas como uma parede, por exemplo, é resultado de interações intermoleculares. Admitindo-se que a parede é recoberta por um material apolar e encontra-se seca, assinale a alternativa que classifica CORRETAMENTE o tipo de interação que prevalece entre as lagartixas e a parede, respectivamente:
A) Íon-íon
B) Íon-dipolo permanente
C) Dipolo induzido-dipolo induzido
D) Dipolo permanente-dipolo induzido
E) Dipolo permanente-dipolo permanente
Questão 07 sobre Interações Intermoleculares: (Unip-SP) O principal tipo de força atrativa que deve ser vencida para sublimar o gelo seco (CO2 sólido) é:
A) ligação covalente.
B) força de London (entre dipolos temporários).
C) força entre dipolos permanentes (devido à diferença de eletronegatividade).
D) ligação coordenada.
E) ligação iônica.
Questão 08. (UFES) A existência de pontes de hidrogênio só é possível entre compostos quando há:
A) um elemento fortemente eletropositivo ligado a um átomo de hidrogênio.
B) dois elementos, um fortemente eletropositivo e outro fortemente eletronegativo, ligados entre si.
C) um elemento fortemente eletronegativo, dotado de pares de elétrons não compartilhados, ligado ao hidrogênio.
D) um aumento muito grande na intensidade das forças de London.
E) uma ligação química entre o hidrogênio e os elementos de transição externa.
Questão 09. (UNIRIO-RJ) A mãe de Joãozinho, ao lavar a roupa do filho após uma festa, encontrou duas manchas na camisa: uma de gordura e outra de açúcar. Ao lavar apenas com água, ela verificou que somente a mancha de açúcar desapareceu completamente. De acordo com a regra segundo a qual “semelhante dissolve semelhante”, indique a alternativa que contém a força intermolecular responsável pela remoção do açúcar na camisa de Joãozinho.
A) Ligação iônica
B) Ligação metálica
C) Ligação covalente polar
D) Forças de London
E) Ponte de hidrogênio
Questão 10 sobre Interações Intermoleculares: (Enem) Leia o texto a seguir:
Tecidos Inteligentes
Os tecidos térmicos são formados por fibras poliméricas cujas forças de atração intermolecular são do tipo ligações de hidrogênio. Quando a temperatura está elevada, há uma ruptura de tais interações e a consequente absorção de energia, diminuindo a temperatura do meio (a pele do usuário). Quando a temperatura está baixa, as interações atrativas são restabelecidas, liberando energia.
Caso utilizássemos um tecido cujas unidades de repetição estivessem unidas por meio de dipolo induzido, o conforto térmico desse tecido:
A) seria mais intenso do que se utilizássemos um tecido cujas unidades de repetição estivessem unidas por meio de dipolos permanentes.
B) seria mais intenso do que se utilizássemos um tecido cujas unidades de repetição estivessem unidas por meio de ligações de hidrogênio.
C) seria igualmente intenso do que se utilizássemos um tecido cujas unidades de repetição estivessem unidas por meio de ligações de hidrogênio.
D) seria menos intenso do que se utilizássemos um tecido cujas unidades de repetição estivessem unidas por meio de ligações covalentes.
E) seria menos intenso do que se utilizássemos um tecido cujas unidades de repetição estivessem unidas por meio de ligações de hidrogênio.
🔵 >>> Confira a lista completa com todos os exercícios de Química.
Gabarito com as respostas da lista de questões de química sobre Interações Intermoleculares:
01. C;
02. E;
03. B;
04. A;
05. C;
06. C;
07. B;
08. C;
09. E;
10. E
Doutorando em Genética e Biologia Molecular – UESC-BA
Mestre em Genética e Biologia Molecular – UESC-BA
Pós-Graduado em Metodologia do Ensino de Biologia e Química – FAEL
Licenciado em Ciências Biologias – IFMT/Campus Juína
