Questão 01 sobre Massa: (Unesp SP/2007/Exatas). O magnésio tem sido utilizado, na indústria, para as mais diversas aplicações. Por ter densidade menor que outros metais, quando presente em ligas metálicas utilizadas em automóveis, o magnésio contribui para a redução de peso, o que torna o automóvel mais econômico. Sabendo-se que de 1 m3 de água do mar é possível retirar 6,75 kg de MgCl2 e que as massas molares de Mg e Cl são, respectivamente, 24,3 g.mol–1 e 35,5 g.mol–1, calcule a massa de magnésio metálico que pode ser obtida a partir de 10 m3 de água do mar.
Questão 02. (Ufv MG/2007) Oxigênio (O2) pode ser obtido em laboratório pelo aquecimento do clorato de potássio (KClO3), conforme equação abaixo representada.
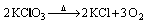
A massa em gramas, aproximada, de oxigênio produzida pela decomposição de 24,5 g de KClO3 é:
a) 9,60
b) 7,20
c) 16,0
d) 3,20
e) 96,0
Questão 03. (Unioeste PR/2007) O processo de fermentação, para a obtenção do etanol, pode ser baseado na reação simplificada, não balanceada, catalisada por leveduras: ![]() .
.
Para que haja a produção de 920 g de etanol, a massa, em gramas, de glicose deve ser
a) 6000.
b) 18000.
c) 600.
d) 1800.
e) 900.
Questão 04 sobre Massa: (Ufsc SC/2007) O químico francês Antoine Lavoisier (1743-1794) realizou uma série de experiências sobre a variação das massas nas reações químicas. Verificou um fato que se repetia também na natureza e concluiu que se tratava de uma lei, que ficou conhecida como Lei da Conservação das Massas, ou Lei de Lavoisier.
Em um experimento realizou-se a combustão completa de magnésio metálico, representada pela equação química não balanceada:
Com relação ao experimento representado acima determine: os coeficientes X, Y e Z (números inteiros), que tornam a equação química corretamente balanceada, e a massa de oxigênio necessária para queimar 60,75 g de magnésio.
Some os resultados numéricos encontrados e assinale no cartão-resposta o valor obtido.
Questão 05. (Ucs RS/2006/Janeiro) Nas viagens espaciais, o dióxido de carbono produzido pela respiração dos astronautas na espaçonave pode ser removido pela reação com óxido de cálcio, o que leva à formação de carbonato de cálcio. Se, durante uma expedição espacial, forem consumidos 28 kg de óxido de cálcio, a massa de dióxido de carbono removida da espaçonave, em valores arredondados, será de
a) 220 g.
b) 22 kg.
c) 11 kg.
d) 34 kg.
e) 150 g.
Questão 06 sobre Massa: (Ucs RS/2006/Julho) O diabetes, uma desordem metabólica, provoca a formação de acetona no sangue. A acetona é um composto volátil e é exalada durante a respiração. Isso faz com que a respiração de uma pessoa diabética, que não está em tratamento, tenha um odor característico. A acetona é produzida pela quebra de gorduras em uma série de reações.
A equação química para a última etapa desse processo é a seguinte:
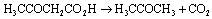
A quantidade de acetona, em valores arredondados, que pode ser produzida a partir de 125 mg do ácido acetoacético é de
a) 71,1 mg.
b) 60,8 mg.
c) 85,5 mg.
d) 53,3 mg.
e) 90,6 mg.
Questão 07. (Fuvest SP/2006/1ªFase) Embalagens de fertilizantes do tipo NPK trazem três números, compostos de dois algarismos, que se referem, respectivamente, ao conteúdo de nitrogênio, fósforo e potássio, presentes no fertilizante. O segundo desses números dá o conteúdo de fósforo, porém expresso como porcentagem, em massa, de pentóxido de fósforo. Para preparar 1 kg de um desses fertilizantes, foram utilizados 558 g de mono-hidrogenofosfato de amônio e 442 g de areia isenta de fosfatos. Na embalagem desse fertilizante, o segundo número, relativo ao fósforo, deve ser, aproximadamente,
Massa molar (g/mol)
mono-hidrogenofosfato de amônio………………………. 132
pentóxido de fósforo …………………………………………. 142
a) 10
b) 20
c) 30
d) 40
e) 50
Questão 08. (Uerj RJ/2006/1ªFase) Em breve, os veículos automotivos poderão utilizar o combustível diesel S-500, menos poluente que o metropolitano por conter menor teor de enxofre.
Observe a tabela a seguir.

A poluição da atmosfera se dá após a transformação do enxofre em dióxido de enxofre, ocorrida na queima de óleo diesel.
A equação química abaixo indica essa transformação.
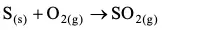
Dois caminhões, um utilizando diesel S-500 e outro, diesel metropolitano, deslocam-se com velocidade média de 50 km/h, durante 20h, consumindo, cada um, 1L de combustível a cada 4 km percorridos.
Considerando as condições acima descritas e a conversão total do enxofre em dióxido de enxofre, a redução da poluição proporcionada pelo caminhão que usa diesel S-500, em relação àquele que usa diesel metropolitano, expressa em gramas de SO2 lançado na atmosfera, corresponde a:
a) 800
b) 600
c) 500
d) 300
Questão 09. (Ufscar SP/2006/1ªFase) O funcionamento de air bag de veículos automotores é baseado na reação química representada pela equação:
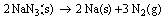
A reação é iniciada por um sensor de choque, e ocorre rapidamente, com o N2 formado preenchendo o air bag em cerca de 0,03 s. O Na(s) formado na reação, por ser muito reativo, é consumido por reação rápida com outro reagente presente na mistura inicial de reagentes. Se no funcionamento de um air bag 130 g de NaN3 forem totalmente decompostos, pode-se afirmar que:
a) serão produzidos 23g de Na(s).
b) serão produzidos 21g de N2(g).
c) serão produzidos 84g de N2(g).
d) o gás produzido ocupará um volume de 22,4 L nas condições normais de pressão e temperatura (CNPT).
e) se o Na(s) formado reagisse com água, a água seria decomposta, liberando oxigênio gasoso e grande quantidade de calor.
Questão 10 sobre Massa: (Efoa MG/2006/1ªFase) Nas estações de tratamento de água, eliminam-se as impurezas sólidas em suspensão através do arraste de flóculos de Al(OH)3, produzidos conforme mostrado pela equação: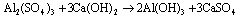
Se para tratar 1.000 L de água forem adicionados 2 kg de Al2(SO4)3, a quantidade de Ca(OH)2 necessária para reagir completamente com esse sal, em kg, é:
a) 1,3
b) 3,1
c) 0,4
d) 9,2
e) 2,0
🔵 >>> Confira a lista completa com todos os exercícios de Química.
Gabarito com as respostas das questões de química sobre Cálculos Estequiométricos Massa:
01. ![]() ;
;
02. A;
03. D;
04. 45;
05. B;
06. A;
07. C;
08. B;
09. C;
10. A
Doutorando em Genética e Biologia Molecular – UESC-BA
Mestre em Genética e Biologia Molecular – UESC-BA
Pós-Graduado em Metodologia do Ensino de Biologia e Química – FAEL
Licenciado em Ciências Biologias – IFMT/Campus Juína
