Questão 01 sobre Propriedades Coligativas das Soluções: Dado o gráfico a seguir,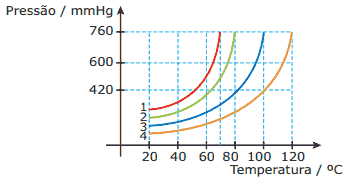
1. n-hexano 2. benzeno 3. água 4. ácido acético
JULGUE os seguintes itens.
( ) A ordem crescente de volatilidade dos líquidos é n-hexano < benzeno < água < ácido acético.
( ) Nas mesmas condições de pressão e temperatura, a substância que sempre terá maior temperatura de ebulição é o ácido acético.
( ) A substância que possui maior pressão máxima de vapor, a qualquer temperatura, é o n-hexano.
( ) A temperatura de ebulição do benzeno, ao nível do mar, é de 80 ºC.
( ) A pressão externa necessária para a água ferver a 60 ºC é de 420 mmHg.
Questão 02. (UEL-PR) Leia as afirmações referentes ao gráfico que representa a variação da pressão de vapor em equilíbrio com a temperatura.
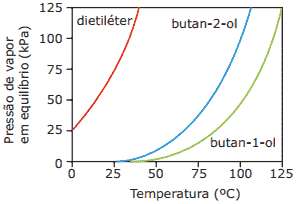
I. As forças de atração intermoleculares das substâncias apresentadas, no estado líquido, aumentam na seguinte ordem: dietiléter < butan-2-ol < butan-1-ol.
II. O ponto de ebulição normal é a temperatura na qual a pressão de vapor do líquido é igual à pressão de uma atmosfera.
III. A pressão de vapor de um líquido depende da temperatura; quanto maior a temperatura, maior a sua pressão de vapor.
IV. À medida que a pressão atmosférica sobre o líquido é diminuída, é necessário elevar a sua temperatura, para que a pressão de vapor se iguale às novas condições do ambiente.
Entre as afirmativas, estão CORRETAS:
A) I, II e IV.
B) I, III, e IV.
C) I, II e III.
D) II, III e IV.
E) I, II, III e IV.
Questão 03 sobre Propriedades Coligativas das Soluções: (PUC RS) Observe a figura a seguir:
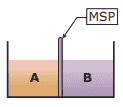
Em que:
A = solução de glicose 0,8 M
B = solução de glicose 0,2 M
MSP = membrana semipermeável
Pela análise da figura, é CORRETO afirmar que, após algum tempo:
A) a solução A ficará mais concentrada.
B) as duas soluções continuarão com a mesma concentração.
C) ocorrerá a diluição da solução B.
D) a solução B ficará mais concentrada.
E) as duas soluções terão a sua concentração aumentada.
Questão 04. (PUCPR) Volumes iguais de duas soluções, sendo uma de glicose (solução X) e outra de sacarose (solução Y), são postos em contato através de uma membrana semipermeável (permeável à água e não permeável à glicose e sacarose).
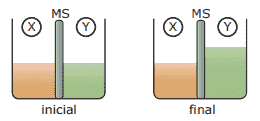
Com o passar do tempo, houve alteração no nível de líquido dos compartimentos, conforme mostrado nos esquemas anteriores. Com base nessas informações, podemos afirmar que:
A) a solução Y é hipotônica em relação a X.
B) a solução Y é mais diluída que X.
C) a solução Y tem maior pressão osmótica que X.
D) a solução X é hipertônica em relação a Y.
E) a solução X tem maior pressão osmótica q
Questão 05 sobre Propriedades Coligativas das Soluções: (CEFET-MG–2011) A extremidade superior de um cilindro de vidro encontra-se aberta, e a inferior, fechada com uma membrana de acetato de celulose. Esse cilindro é preenchido com uma solução aquosa de propan-2-ol a 50% V/V e, em seguida, é colocado em um copo contendo água, como mostra a figura seguinte.
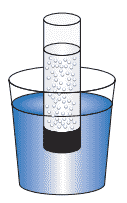
Sabendo-se que o acetato de celulose é permeável às moléculas de volume igual ou menor que a água, é INCORRETO afirmar que a(o):
A) volume contido no copo reduz ao longo do tempo.
B) concentração de álcool no cilindro diminui com o tempo.
C) propan-2-ol pode ser purificado se a osmose for reversa.
D) pressão de vapor no copo é igual à do cilindro se o volume do sistema for constante.
E) força exercida sobre a superfície da mistura é equivalente à pressão atmosférica.
Questão 06. (VUNESP) Isolou-se uma proteína de uma amostra de soro sanguíneo. Uma dispersão coloidal de 685 mg da referida proteína, em água suficiente para formar 10,0 mL de solução, tem uma pressão osmótica de 0,28 atm a 7 ºC (R = 0,082 L.atm.mol-1.K-1). Considerando a proteína como sendo um composto covalente típico, sua massa molecular é:
A) 5,6×103 g.mol-1.
B) 685 g.mol-1.
C) 6×1023 g.mol-1.
D) 12×10-3 g.mol-1.
E) 12×103 g.mol-1.
Questão 07. (Enem–1999) A panela de pressão permite que os alimentos sejam cozidos em água muito mais rapidamente do que em panelas convencionais. Sua tampa possui uma borracha de vedação que não deixa o vapor escapar, a não ser através de um orifício central sobre o qual assenta um peso que controla a pressão. Quando em uso, desenvolve-se uma pressão elevada no seu interior. Para a sua operação segura, é necessário observar a limpeza do orifício central e a existência de uma válvula de segurança, normalmente situada na tampa.
O esquema da panela de pressão e um diagrama de fase da água são apresentados a seguir.
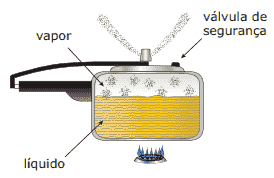
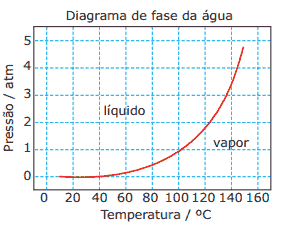
A vantagem do uso de panela de pressão é a rapidez para o cozimento de alimentos, e isso se deve à:
A) pressão no seu interior, que é igual à pressão externa.
B) temperatura de seu interior, que está acima da temperatura de ebulição da água no local.
C) quantidade de calor adicional que é transferida à panela.
D) quantidade de vapor que está sendo liberada pela válvula.
E) espessura da sua parede, que é maior que a das panelas comuns.
Questão 08 sobre Propriedades Coligativas das Soluções: (Enem–1999) Em nosso planeta, a quantidade de água está estimada em 1,36×106 trilhões de toneladas. Desse total, calcula-se que cerca de 95% são de água salgada e dos 5% restantes, quase a metade, está retida nos polos e geleiras.
O uso de água do mar para obtenção de água potável ainda não é realidade em larga escala. Isso porque, entre outras razões:
A) o custo dos processos tecnológicos de dessalinização é muito alto.
B) não se sabe como separar adequadamente os sais nela dissolvidos.
C) comprometeria muito a vida aquática dos oceanos.
D) a água do mar possui materiais irremovíveis.
E) a água salgada do mar tem temperatura de ebulição alta.
Questão 09. (Enem–1998) A tabela a seguir registra a pressão atmosférica em diferentes altitudes, e o gráfico relaciona a pressão de vapor da água em função da temperatura.
| Altitude (Km) | Pressão Atmosférica (mmHg) |
| 0 | 760 |
| 1 | 600 |
| 2 | 480 |
| 4 | 300 |
| 6 | 170 |
| 8 | 120 |
| 10 | 100 |
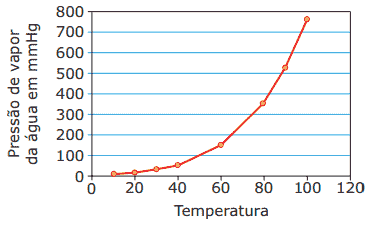
| Natal (RN) | Nível do mar |
| Campos do Jordão (SP) | altitude 1628m |
| Pico da Neblina (PR) | altitude 3014m |
A temperatura de ebulição será:
A) maior em Campos do Jordão.
B) menor em Natal.
C) menor no Pico da Neblina.
D) igual em Campos do Jordão e Natal.
E) não dependerá da altitude.
Questão 10. (Enem–2006) O Aquífero Guarani, mega reservatório hídrico subterrâneo da América do Sul, com 1,2 milhão de km2, não é o “mar de água doce” que se pensava existir.
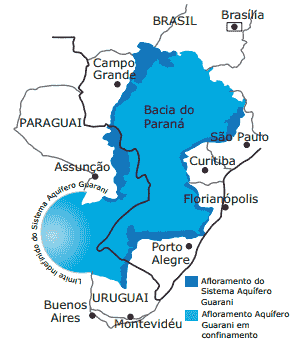
Enquanto em algumas áreas a água é excelente, em outras, é inacessível, escassa ou não potável. O aquífero pode ser dividido em quatro grandes compartimentos. No compartimento Oeste, há boas condições estruturais que proporcionam recarga rápida a partir das chuvas e as águas são, em geral, de boa qualidade e potáveis. Já no compartimento Norte-Alto Uruguai, o sistema encontra-se coberto por rochas vulcânicas a profundidades que variam de 350 m a 1 200 m. Suas águas são muito antigas, datando da Era Mesozoica, e não são potáveis em grande parte da área, com elevada salinidade, sendo que os altos teores de fluoretos e de sódio podem causar alcalinização do solo.
SCIENTIFIC AMERICAN BRASIL, n. 47, abr. 2006 (Adaptação).
Em relação ao aquífero Guarani, é correto afirmar que:
A) seus depósitos não participam do ciclo de água.
B) águas provenientes de qualquer um de seus compartimentos solidificam-se a 0 ºC.
C) é necessário, para utilização de seu potencial como reservatório de água potável, conhecer detalhadamente o aquífero.
D) a água é adequada ao consumo humano direto em grande parte da área do compartimento Norte-Alto Uruguai.
E) o uso das águas do compartimento Norte-Alto Uruguai para irrigação deixaria ácido o solo.
Questão 11 sobre Propriedades Coligativas das Soluções: (UCDB-MT) As propriedades coligativas das soluções dependem:
a) Da pressão máxima de vapor do líquido.
b) Da natureza das partículas dispersas na solução.
c) Da natureza do solvente, somente.
d) Do número de partículas dispersas na solução.
e) Da temperatura de ebulição do líquido.
🔵 >>> Confira a lista completa com todos os exercícios de Química.
Gabarito com as respostas do simulado com exercícios de química sobre as Propriedades Coligativas das Soluções:
01. F, V, V, V, F;
02. C;
03. D;
04. C;
05. D;
06. A;
07. B;
08. A;
09. C;
10. C;
11. D
Doutorando em Genética e Biologia Molecular – UESC-BA
Mestre em Genética e Biologia Molecular – UESC-BA
Pós-Graduado em Metodologia do Ensino de Biologia e Química – FAEL
Licenciado em Ciências Biologias – IFMT/Campus Juína
