Questão 01 sobre Densidade e Mudanças de Estado Físico: (UnB-DF) Considere quantidades iguais de água nos três estados físicos (s = sólido; l = líquido; g = gasoso) relacionados no esquema a seguir: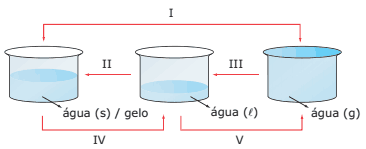
Julgue os itens.
( ) O processo I é denominado condensação.
( ) O processo II envolve absorção de energia.
( ) O processo III é acompanhado por uma diminuição de densidade.
( ) O processo IV é denominado vaporização.
( ) Um aumento de pressão sob temperatura constante provocaria igual decréscimo de volume de água líquida e gasosa.
( ) O vapor-d’água está em um estado menos energético do que a água líquida e sólida.
Questão 02. (ENADE) A densidade dos fluidos supercríticos é da mesma ordem de grandeza da densidade dos líquidos, enquanto sua viscosidade e sua difusibilidade são maiores que a dos gases, porém menores que a dos líquidos. É bastante promissora a substituição de solventes orgânicos por CO2 supercrítico em extrações. O ponto triplo no diagrama de fases do CO2, bem como sua região supercrítica, são apresentados no diagrama mostrado a seguir:
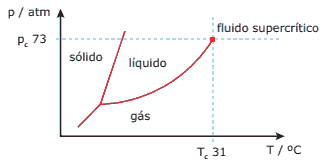
Considerando as informações contidas no diagrama de fases do CO2, analise as afirmações a seguir:
I. As fases sólida, líquida e gasosa encontram-se em equilíbrio no ponto triplo.
II. As fases líquida e gasosa encontram-se em equilíbrio na região supercrítica.
III. Em temperaturas acima de 31 ºC, não será possível liquefazer o CO2 supercrítico por compressão.
IV. Em pressões acima de 73 atm, o CO2 só será encontrado no estado sólido.
São CORRETAS apenas as afirmações:
A) I e II.
B) I e III.
C) I e IV.
D) II e III.
E) II e IV.
Questão 03. (UFMG) A tabela a seguir contém propriedades de algumas substâncias.
| Substância | T.F. / ºC | T.E. / ºC | d / g.mL–1 | Solubilidade em água |
| Glicerina | 20 | 290 | 1,26 | muito solúvel |
| Eugenol | –7,5 | 253 | 1,07 | insolúvel |
| Etanotiol | –144 | 35 | 0,839 | pouco solúvel |
Com base nos dados da tabela, é possível concluir que todas as alternativas a seguir estão corretas, EXCETO:
A) A mistura eugenol-glicerina pode ser separada por adição de água.
B) Numa mistura de água e glicerina, a água é o sobrenadante.
C) Um litro de glicerina pesa tanto quanto 1,26 litro de água.
D) O etanotiol é um líquido mais volátil do que a água.
E) Num dia muito frio, a glicerina é um sólido.
Questão 04 sobre Densidade e Mudanças de Estado Físico: (Unicamp-SP–2008) Depois das 19 horas, os convidados começaram a chegar. Dina os recepcionava no bar, onde havia dois baldes: um deles com gelo e o outro com gelo seco. Dina bradava aos quatro cantos: “Isto faz a festa tornar-se mais química, já que esses sólidos serão usados para resfriar as bebidas!” Para cada bebida, Estrondosa escolhia o sólido mais apropriado. Curiosamente, alguém pediu duas doses iguais de uísque, uma com gelo e outra com gelo seco, mas colocou os copos em uma mesa e não consumiu as bebidas. Passado um certo tempo, um colega de faculdade resolveu verificar se Dina ainda era a “sabichona” de antigamente, e foi logo perguntando:
A) “Esses sólidos, quando colocados nas bebidas, sofrem transformações. Que nomes são dados para essas duas transformações? E por que essas transformações fazem com que as bebidas se resfriem?”
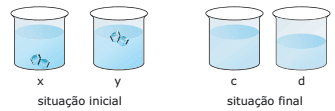
B) “Dina, veja essas figuras e pense naqueles dois copos de uísque que nosso amigo não bebeu. Qual copo, da situação inicial, corresponde ao copo da situação final? Em algum dos copos, a concentração final de álcool ficou diferente da concentração inicial? Por quê?“ Observação: Considerar as figuras para responder ao item B.
Questão 05. (UEL-PR) Propriedades físicas como densidade, ponto de fusão e ponto de ebulição são importantes para identificar e diferenciar quando um sistema é composto de uma substância pura ou por uma mistura. Analise os gráficos a seguir, que representam mudanças de estado físico.
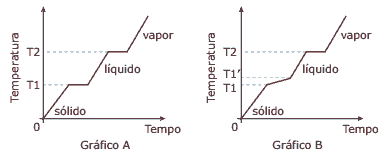
Em relação às mudanças de estado físico, é CORRETO afirmar:
A) O segmento T1–T1’ no gráfico B caracteriza uma substância pura.
B) O gráfico A representa a mudança de estado físico de uma mistura eutética.
C) O gráfico B representa a mudança de estado físico de uma mistura azeotrópica.
D) O gráfico A representa a mudança de estado físico de uma mistura trifásica.
E) O gráfico B representa a mudança de estado físico de uma mistura que apresenta ponto de ebulição não definido.
Questão 06. (UFSM-RS) Para acelerar o processo de evaporação na secagem de grãos, utiliza-se um jato de ar a uma temperatura mais elevada do que a do meio ambiente.
Então, sobre o processo de evaporação, é possível afirmar.
I. Ocorre a qualquer temperatura e é tanto mais rápido quanto mais elevada a temperatura do líquido.
II. Fica mais rápido se o vapor do líquido é removido das proximidades do líquido restante.
III. A quantidade de líquido evaporada por unidade de tempo independe da área da superfície livre do líquido.
Está(ão) CORRETA(S):
A) apenas I.
B) apenas I e II.
C) apenas III.
D) apenas II e III.
E) I, II e III.
Questão 07 sobre Densidade e Mudanças de Estado Físico: (UFJF-MG) Atualmente, é comum encontrar, nas prateleiras de supermercados, alimentos desidratados, isto é, isentos de água em sua composição. O processo utilizado na desidratação dos alimentos é a liofilização. A liofilização consiste em congelar o alimento a uma temperatura de –197 ºC e depois submeter o alimento congelado a pressões muito baixas. Na temperatura de –197 ºC, a água contida no alimento encontra-se no estado sólido e, com o abaixamento de pressão, passa diretamente para o estado de vapor, sendo então eliminada. Assinale a afirmação CORRETA.
A) No processo de liofilização, a água passa por uma transformação química, produzindo H2 e O2, que são gases.
B) No processo de liofilização, a água passa por um processo físico conhecido como evaporação.
C) No processo de liofilização, o alimento sofre decomposição, perdendo água.
D) No processo de liofilização, a água sofre decomposição.
E) No processo de liofilização, a água passa por uma transformação física denominada sublimação.
Questão 08. (PUC Minas–2007) Considere o quadro a seguir, que apresenta algumas substâncias e suas respectivas temperaturas de fusão (T.F.) e de ebulição (T.E.), ao nível do mar.
| Substância | T.F. / ºC | T.E. / ºC |
| Água | 0 | 100,0 |
| Clorofórmio | –63,0 | 62,3 |
| Hidróxido de sódio | 318,6 | 1 389,0 |
| Ácido acético | 16,7 | 118,1 |
Considerando-se esses dados, é INCORRETO afirmar:
A) O clorofórmio a 70 ºC é gasoso.
B) A 85 ºC, o hidróxido de sódio é sólido.
C) A 25 ºC, duas das substâncias são líquidas.
D) A substância mais volátil é o clorofórmio.
Questão 09. (Fatec-SP–2006) Duas amostras de naftalina, uma de 20,0 g (amostra A) e outra de 40,0 g (amostra B), foram colocadas em tubos de ensaio separados, para serem submetidas à fusão. Ambas as amostras foram aquecidas por uma mesma fonte de calor. No decorrer do aquecimento de cada uma delas, as temperaturas foram anotadas de 30 em 30 segundos. Um estudante, considerando tal procedimento, fez as seguintes previsões:
I. A fusão da amostra A deve ocorrer a temperatura mais baixa do que a da amostra B.
II. A temperatura de fusão da amostra B deve ser o dobro da temperatura de fusão da amostra A.
III. A amostra A alcançará a temperatura de fusão num tempo menor que a amostra B.
IV. Ambas as amostras devem entrar em fusão à mesma temperatura.
É CORRETO o que se afirma apenas em:
A) I.
B) II.
C) III.
D) II e III.
E) III e IV.
Questão 10 sobre Densidade e Mudanças de Estado Físico: (UFU-MG–2008) O gráfico a seguir representa a curva de aquecimento de uma substância à pressão constante de 1 atm.
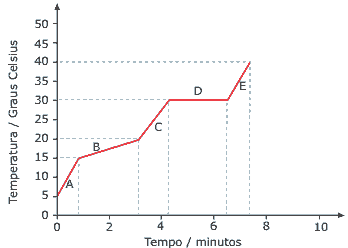
Pede-se:
A) Quais são os estados físicos dessa substância indicados pelas letras A, C e E?
B) EXPLIQUE o fenômeno que ocorre na região indicada pela letra D.
C) Qual é o ponto de ebulição dessa substância em ºC?
D) Qual é o intervalo de temperatura em ºC no qual estará o ponto de fusão dessa substância?
🔵 >>> Confira a lista completa com todos os exercícios de Química.
Gabarito com as respostas das atividades de química sobre Densidade e Mudanças de Estado Físico:
01. F, F, F, F, F, F;
02. B;
03. B;
04. A) O gelo sofre fusão: H2O(s) → H2O(l)
O gelo seco sofre sublimação: CO2(s) → CO2(g)
Essas transformações físicas esfriam as bebidas porque são endotérmicas, isto é, absorvem calor dos líquidos, diminuindo suas temperaturas.
B) O copo d corresponde ao copo x da condição inicial, pois seu volume é menor que o do copo c, onde foi colocado o gelo (flutuação).
Os cubos sólidos que afundam (gelo seco) estão no copo x.
Sim, no copo y, onde havia gelo no início (copo c). A água líquida que se formou diluiu o álcool da bebida original.
05. C;
06. B;
07. E;
08. C;
09. E;
10. A) A: sólido
C: líquido
E: gás
B) Vaporização ou ebulição. Passagem do estado líquido para o gasoso.
C) 30 ºC
D) Entre 15 e 20 ºC
Doutorando em Genética e Biologia Molecular – UESC-BA
Mestre em Genética e Biologia Molecular – UESC-BA
Pós-Graduado em Metodologia do Ensino de Biologia e Química – FAEL
Licenciado em Ciências Biologias – IFMT/Campus Juína
