Questão 01 sobre Termodinâmica: U.F. Santa Maria-RS – As variáveis que podem definir os estados possíveis para 1 mol de gás ideal são:
a) calor, massa e volume;
b) temperatura, densidade e pressão;
c) temperatura, pressão e volume;
d) densidade, pressão e calor;
e) densidade, massa e calor.
Questão 02. UFMT – Considere as seguintes situações que ocorrem no laboratório de uma escola:
a) Uma garrafa bem arrolhada cheia de gás sulfídrico é tirada do armário e exposta ao Sol. Sua temperatura, então, começa a aumentar.
b) Um estudante despeja areia lentamente sobre o êmbolo de um cilindro que contém oxigênio, comprimindo-o.
Em relação ao comportamento dos gases, julgue os itens.
( ) Em A, o volume permanece constante, mas a pressão vai aumentando, o que caracteriza uma transformação isovolumétrica.
( ) Em A, ocorre uma diminuição na média de colisões das moléculas de gás com as paredes da garrafa.
( ) Na situação B, trata-se de uma transformação isotérmica, pois o volume do gás varia inversamente à pressão exercida sobre ele.
( ) A equação pV = nRT descreve exatamente os comportamentos dos gases em A e B.
( ) Os gases reais podem ser considerados gases perfeitos sempre que submetidos a grandes temperaturas e baixas pressões.
Questão 03. UESC-BA – O equivalente mecânico do calor, medido por James P Joule em 1843, refere-se à relação entre as unidades de medida caloria e joule, isto é, 1cal = 4,18J.
Para chegar à essa relação, Joule considerou que:
01) o aquecimento leva um sólido a dilatar-se em todas as direções;
02) a absorção de calor produz, necessariamente, elevação da temperatura de um corpo;
03) o calor e a energia mecânica têm a mesma natureza;
04) o calor pode ser usado para produzir vapor;
05) o calor é capaz de realizar trabalho mecânico no interior de uma máquina térmica.
Questão 04 sobre Termodinâmica: UESC-BA – Num processo termodinâmico, a variação da energia interna sofrida por um gás é conseqüência do balanço energético entre as grandezas físicas:
01) quantidade de calor e trabalho;
02) temperatura e quantidade de calor;
03) trabalho e pressão;
04) volume e temperatura;
05) pressão e volume.
Questão 05. U.E. Ponta Grossa-PR – A figura abaixo mostra dois momentos de um cilindro metálico dotado de um êmbolo, em cujo interior se encontra um gás encerrado em equilíbrio. No segundo momento, o gás recebe uma quantidade de calor Q. Sobre este evento, assinale o que for correto.
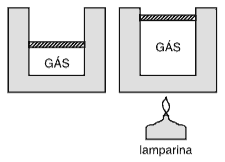
01. O calor, isoladamente, descreve o estado do sistema.
02. As variáveis de estado (PVT) descrevem os estados de equilíbrio do sistema.
04. No segundo momento, o aumento do volume do gás torna o trabalho nulo. 08. O calor e o trabalho descrevem as transformações do sistema.
16. O gás contido no sistema é veículo para a realização de trabalho.
Dê, como resposta, a soma das alternativas corretas.
Questão 06. UFR-RJ – A primeira Lei da Termodinâmica, denominada Lei da Conservação da Ener-gia estabelece: “A energia do Universo é constante”.
Num sistema que realiza um trabalho de 125 J, absorvendo 75 J de calor, a variação de energia é igual a:
a) –125J
b) – 75 J
c) – 50 J
d) 75 J
e) 200 J
Questão 07 sobre Termodinâmica: U. Alfenas-MG – Considere as proposições abaixo:
I. O perfume comprimido num spray esfria quando expandido, pois a energia interna diminui, fazendo diminuir a temperatura.
II. É possível aquecer um gás sem fornecer-lhe calor.
III. É possível fornecer calor a um gás e este ficar mais frio.
IV. Numa transformação qualquer, o trabalho é numericamente igual à área correspondente num diagrama da temperatura pelo volume.
Estão corretas:
a) todas
b) somente I e IV
c) somente I, II e III
d) somente I, III e IV
e) somente II e IV
Questão 08. PUC-RS – Em relação a comportamentos termodinâmicos de materiais e substâncias, é correto afirmar que:
a) dois corpos de mesma massa sempre têm a mesma capacidade térmica;
b) o calor específico de uma substância é constante, independentemente da fase em que ela se encontre;
c) na compressão adiabática de um gás, sua energia interna permanece constante;
d) na transformação isovolumétrica de um gás, este realiza trabalho;
e) a energia interna de um sistema depende da quantidade de partículas que ele possui.
Questão 09. UFMS – O gráfico abaixo representa duas curvas isotérmicas relacionadas a um gás ideal contido em um recipiente que pode variar o seu volume. Desse modo, é correto afirmar que: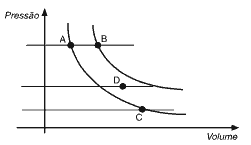
01. se o gás for submetido a um processo termodinâmico partindo do estado A para o estado B, a pressão do gás não varia e sua energia interna aumenta.
02. se o gás for submetido a um processo termodinâmico partindo do estado A para o estado D, a sua energia interna não varia.
04. se o gás for submetido a um processo termodinâmico partindo do estado A para o estado C, a temperatura do gás não varia e não haverá troca de calor com o ambiente.
08. se o gás passar por um processo termodinâmico partindo do estado A, passando pelos estados D e C e retornando ao estado A, a quantidade de calor trocada com o ambiente é igual ao trabalho realizado pelo gás.
16. se o gás passar por um processo termodinâmico partindo do estado A para o estado C e retornando ao estado A pelo mesmo caminho, o trabalho total realizado pelo gás é nulo. Dê, como resposta, a soma das afirmativas corretas.
Questão 10 sobre Termodinâmica: UFRS – Um recipiente hermeticamente fechado, de paredes rígidas e permeáveis à passagem de calor, contém uma certa quantidade de gás à temperatura absoluta T.
Selecione a alternativa que preenche corretamente as lacunas no parágrafo abaixo, na ordem em que elas aparecem.
Se o recipiente for mergulhado em um tanque contendo um líquido à temperatura absoluta 2T, a temperatura do gás ……………, e sua energia interna …………….
a) diminuirá – diminuirá
b) diminuirá – permanecerá constante
c) permanecerá constante – aumentará d) aumentará – aumentará
e) aumentará – permanecerá constante
🔵 >>> Verifique todos os nossos exercícios e atividades de Física.
Gabarito com as respostas da lista de exercícios de Física sobre Termodinâmica:
01. c;
02. V – F –V – F –V;
03. 03;
04. 01;
05. 26;
06. c;
07. c;
08. e;
09. 01 + 08 + 16;
10. d
Doutorando em Genética e Biologia Molecular – UESC-BA
Mestre em Genética e Biologia Molecular – UESC-BA
Pós-Graduado em Metodologia do Ensino de Biologia e Química – FAEL
Licenciado em Ciências Biologias – IFMT/Campus Juína
