Questão 01 sobre as Leis da Termodinâmica: (Urca-CE) A primeira lei da termodinâmica está intimamente relacionada com:
a) O princípio da conservação da quantidade de movimento dos sistemas de partículas.
b) A lei da dilatação térmica
c) O princípio da conservação da energia.
d) A lei dos gases ideais.
e) O aumento da entropia do Universo
Questão 02. Uma fonte térmica fornece 300J de calor a um sistema gasoso. Parte dessa energia (220J) é transformada em trabalho, fazendo com que o sistema gasoso sofra uma expansão.
Determine a variação da energia interna do sistema gasoso.
Questão 03. Modelo Enem. O gráfico abaixo mostra a variação do volume em função da temperatura de um gás ideal que sofreu uma transformação à pressão constante de P = 120 N/m2. A quantidade de calor recebida pelo gás durante o processo foi de 800 joules.
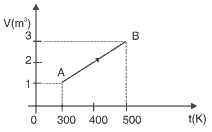
Com os dados, pode-se dizer que a variação da energia interna que este gás sofreu foi de:
a) 560 joules.
b) 260 joules.
c) 300 joules.
d) 480 joules.
e) 580 joules.
Questão 04 sobre as Leis da Termodinâmica: Modelo Enem. O gráfico abaixo representa duas curvas isotérmicas relacionadas a um gás ideal contido em um recipiente que pode variar o seu volume. Desse modo, é correto afirmar que:
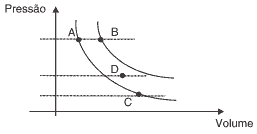
(01) se o gás for submetido a um processo termodinâmico partindo do estado A para o estado B, a pressão do gás não varia e sua energia interna aumenta.
(02) se o gás for submetido a um processo termodinâmico partindo do estado A para o estado D, a sua energia interna não varia.
(04) se o gás for submetido a um processo termodinâmico partindo do estado A para o estado C, a temperatura do gás não varia e não haverá troca de calor com o ambiente.
(08) se o gás passar por um processo termodinâmico partindo do estado A, passando pelos estados D e C e retornando ao estado A, a quantidade de calor trocada com o ambiente é igual ao trabalho realizado pelo gás.
(16) se o gás passar por um processo termodinâmico partindo do estado A para o estado C e retornando ao estado A pelo mesmo caminho, o trabalho total realizado pelo gás.
Questão 05. Modelo Enem. Em um processo termodinâmico, uma quantidade de n moles de um gás ideal é aquecida por uma quantidade de calor Q = 1000 J e realiza trabalho igual a W. Ao fim do processo termodinâmico , o sistema retorna à temperatura inicial, ou seja, à energia inicial.
Calcule o trabalho realizado.
a) -1000 J.
b) 0 J.
c) 2000 J.
d) 1000 J.
e) 500 J.
Questão 06. Modelo Enem. Durante determinado intervalo de tempo, uma máquina térmica recebe 1.200J de calor de uma fonte quente e transfere 900J para uma fonte fria. Com relação ao funcionamento dessa máquina, calcule:
a) O trabalho realizado;
b) O rendimento.
Questão 07 sobre as Leis da Termodinâmica: (Uem) Um cilindro com pistão, contendo uma amostra de gás ideal, comprime a amostra de maneira que a temperatura, tanto do cilindro com pistão quanto da amostra de gás ideal, não varia.
O valor absoluto do trabalho realizado nessa compressão é de 400 J. Sobre o exposto, assinale o que for correto.
01) O trabalho é positivo, pois foi realizado sobre o gás.
02) A transformação é denominada adiabática.
04) A energia interna do gás aumentou, pois este teve seu volume diminuído.
08) O gás ideal cedeu uma certa quantidade de calor à vizinhança.
16) A quantidade de calor envolvida na compressão de gás foi de 200 J.
Questão 08. (Uem) Assinale o que for correto.
01) A energia interna total permanece constante em um sistema termodinâmico isolado.
02) Quando um sistema termodinâmico recebe calor, a variação na quantidade de calor que este possui é positiva.
04) O trabalho é positivo, quando é realizado por um agente externo sobre o sistema termodinâmico, e negativo, quando é realizado pelo próprio sistema.
08) Não ocorre troca de calor entre o sistema termodinâmico e o meio, em uma transformação adiabática.
16) Não ocorre variação da energia interna de um sistema termodinâmico, em uma transformação isotérmica.
Questão 09. (Unesp) Um recipiente contendo um certo gás tem seu volume aumentado graças ao trabalho de 1664 J realizado pelo gás. Neste processo, não houve troca de calor entre o gás, as paredes e o meio exterior. Considerando que o gás seja ideal, a energia de 1 mol desse gás e a sua temperatura obedecem à relação U = 20,8 T, onde a temperatura T é medida em kelvin e a energia U em joule.
Pode-se afirmar que nessa transformação a variação de temperatura de um mol desse gás, em kelvin, foi de:
a) 50.
b) – 60.
c) – 80.
d) 100.
e) 90.
Questão 10 sobre as Leis da Termodinâmica: (Unicamp) Um gás ideal sofre uma compressão isobárica sob a pressão de 4 . 10-3 N/m2 e o seu volume diminui 0,2 m3. Durante o processo, o gás perde 1,8 . 103 J de calor. A variação da energia interna do gás foi de:
a) 1,8 . 103 J
b) 1,0 . 103 J
c) –8,0 . 103 J
d) –1,0 . 103 J
e) –1,8 . 103 J
🔵 >>> Verifique todos os nossos exercícios e atividades de Física.
Gabarito com as respostas dos exercícios de física sobre as Leis da Termodinâmica:
01. c;
02. DU = 80 K;
03. b;
04. (01 + 08 + 16. = 25;
05. d;
06. a. 300 J b. 25%;
07. 08.
01. Incorreta. Pela convenção de sinais da 1ª lei da termodinâmica, quando se realiza trabalho (W. sobre o gás, esse trabalho é negativo (W = –400 J..
02. Incorreta. A temperatura é constante, portanto, a transformação é isotérmica.
04. Incorreta. A energia interna é função exclusiva da temperatura. Se a transformação é isotérmica a energia interna é constante (DU = 0..
08. Correta. Da 1ª lei da termodinâmica: Como o sinal do calor é negativo, de acordo com a convenção de sinais, o gás cedeu calor à vizinhança.
16. Incorreta. De acordo com o exposto na afirmativa anterior: Q = –400 J.
08. 01 + 02 + 08 + 16 = 27
01. Correto. Sua temperatura não varia
02. Correto. Se não houver variação de volume a temperatura aumenta.
04. Errado. O trabalho é positivo quando o sistema realiza (expansão. e negativo quando realizado sobre ele (contração..
08. Correto. Por definição de adiabática.
16. Correto. A temperatura não varia.
09. c;
10. d;
Doutorando em Genética e Biologia Molecular – UESC-BA
Mestre em Genética e Biologia Molecular – UESC-BA
Pós-Graduado em Metodologia do Ensino de Biologia e Química – FAEL
Licenciado em Ciências Biologias – IFMT/Campus Juína
