Questão 01 sobre Ligações Iônicas: (Unesp) Tem-se dois elementos químicos A e B, com números atômicos iguais a 20 e 35, respectivamente.
a) Escrever as configurações eletrônicas dos dois elementos. Com base nas configurações, dizer a que grupo de tabela periódica pertence cada um dos elementos em questão.
b) Qual será a fórmula do composto formado entre os elementos A e B? Que tipo de ligação existirá entre A e B no composto formado? Justificar.
Questão 02. (Unitau/2015) A hemoglobina humana é uma proteína conjugada formada por Heme (grupo prostético) e globina (proteína). Na oxihemoglobina (figura abaixo), o Fe2+ aparece ligado ao resíduo de histidina da globina, aos quatro nitrogênios do grupo Heme e ao oxigênio molecular.
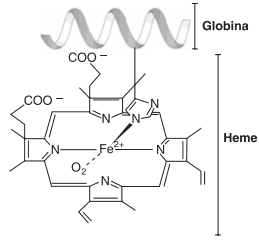
Com base na configuração eletrônica do Fe2+, explique:
a) o(s) tipo(s) de ligação que o Fe2+ faz na estrutura da oxihemoglobina.
b) por que o Fe2+ pode formar 6 ligações.
Questão 03 sobre Ligações Iônicas: (PUC-MG) Analise as seguintes afirmações:
I. Os cátions dos metais alcalinos, alcalino-terrosos e alumínio têm oito elétrons na última (mais externa) camada eletrônica.
II. Os cátions de metais alcalinos, alcalino-terrosos e alumínio têm configuração eletrônica estável.
III. Na formação da ligação iônica, quando um átomo recebe elétrons(s), transforma-se num ânion com configuração eletrônica semelhante à de um gás nobre.
IV. Na formação da ligação iônica, quando um átomo de metal cede elétron(s), transforma-se num cátion com configuração eletrônica semelhante à de um gás nobre.
São afirmativas CORRETAS:
a) I, II e III.
b) I e III apenas.
c) II, III e IV.
d) II e III apenas.
Questão 04. (Espcex (Aman) 2016) Compostos iônicos são aqueles que apresentam ligação iônica. A ligação iônica é a ligação entre íons positivos e negativos, unidos por forças de atração eletrostática.
(Texto adaptado de: Usberco, João e Salvador, Edgard, Química: química geral, vol 1, pág 225, Saraiva, 2009).
Sobre as propriedades e características de compostos iônicos são feitas as seguintes afirmativas:
I. apresentam brilho metálico.
II. apresentam elevadas temperaturas de fusão e ebulição.
III. apresentam boa condutibilidade elétrica quando em solução aquosa.
IV. são sólidos nas condições ambiente (25°C e 1 atm).
V. são pouco solúveis em solventes polares como a água.
Das afirmativas apresentadas estão corretas apenas
a) II, IV e V.
b) II, III e IV.
c) I, III e V.
d) I, IV e V.
e) I, II e III.
Questão 05 sobre Ligações Iônicas: (Mackenzie) Se comparado à água, o cloreto de sódio possui ponto de fusão _______, em consequência da _______ entre _______ .
Os termos que preenchem correta e ordenadamente as lacunas acima são:
(Dados os números atômicos: Na = 11 e Cl = 17)
a) elevado – forte atração – suas moléculas
b) mais baixo – fraca atração – seus íons
c) mais elevado – fraca atração – seus átomos
d) muito baixo – forte atração – seus íons
e) elevado – forte atração – seus íons
Questão 06. (UERJ/2015) Em fins do século XVI, foi feita uma das primeiras aplicações práticas de uma pilha: a decomposição da água em oxigênio e hidrogênio, processo denominado eletrólise. Já que naquela época, com base nesse experimento, sugeriu-se que as forças responsáveis pelas ligações químicas apresentam a seguinte natureza:
a) nuclear
b) elétrica
c) magnética
d) gravitacional
Questão 07 sobre Ligações Iônicas: (Mackenzie) A fórmula do composto e o tipo de ligação que ocorre quando se combinam átomos dos elementos químicos Ba (Z = 56) e Cl (Z = 17) são, respectivamente:
a) Ba2 Cl e dativa.
b) Ba Cl e iônica.
c) Ba2 Cl e covalente normal.
d) Ba Cl2 e iônica.
e) Ba Cl e covalente normal.
Questão 08. (Fatec) Sólidos cristalinos com pontos de ebulição e fusão altos, solúveis em solventes polares e que conduzem corrente elétrica quando fundidos ou em solução, são exemplos de compostos formados por meio de ligação:
a) covalente polar.
b) covalente apolar.
c) covalente dativa.
d) iônica.
e) metálica.
Questão 09. (Fatec) A propriedade que pode ser atribuída à maioria dos compostos iônicos (isto é, aos compostos caracterizados predominantemente por ligações iônicas entre as partículas) é:
a) dissolvidos em água, formam soluções ácidas.
b) dissolvem-se bem em gasolina, diminuindo sua octanagem.
c) fundidos (isto é, no estado líquido), conduzem corrente elétrica.
d) possuem baixos pontos de fusão e ebulição.
e) são moles, quebradiços e cristalinos.
Questão 10 sobre Ligações Iônicas: (Puccamp) Os átomos de certo elemento metálico possuem, cada um, 3 prótons, 4 nêutrons e 3 elétrons. A energia de ionização desse elemento está entre as mais baixas dos elementos da tabela periódica. Ao interagir com halogênio, esses átomos têm alterado o seu número de:
a) prótons, transformando-se em cátions.
b) elétrons, transformando-se em ânions.
c) nêutrons, mantendo-se eletricamente neutros.
d) prótons, transformando-se em ânions.
e) elétrons, transformando-se em cátions.
🔵 >>> Confira a lista completa com todos os exercícios de Química.
Gabarito com as respostas da lista de exercícios de química sobre Ligações Iônicas:
01. a) A: 1s22s22p63s23p64s2 (grupo IIA)
B: 1s22s22p63s23p64s23d104p5 (grupo VIIA)
b) AB2 → ligação iônica, onde A = metal e B = ametal.
02. a. Ligação Iônica
b. Expansão da Camada de Valência
03. d;
04. b;
05. e;
06. b;
07. d;
08. d;
09. c;
10. e
Doutorando em Genética e Biologia Molecular – UESC-BA
Mestre em Genética e Biologia Molecular – UESC-BA
Pós-Graduado em Metodologia do Ensino de Biologia e Química – FAEL
Licenciado em Ciências Biologias – IFMT/Campus Juína
