Questão 01 sobre Misturas Gasosas, Efusão e Difusão: (Enem–2000) A adaptação dos integrantes da seleção brasileira de futebol à altitude de La Paz foi muito comentada em 1995, por ocasião de um torneio, como pode ser lido no texto a seguir.
ATENÇÃO!!! O Gabarito encontra-se no final da página!!!
A seleção brasileira embarca hoje para La Paz, capital da Bolívia, situada a 3 700 metros de altitude, onde disputará o torneio Interamérica. A adaptação deverá ocorrer em um prazo de 10 dias, aproximadamente. O organismo humano, em altitudes elevadas, necessita desse tempo para se adaptar, evitando-se, assim, risco de um colapso circulatório.
PLACAR, edição fev. 1995 (Adaptação).
A adaptação da equipe foi necessária principalmente porque a atmosfera de La Paz, quando comparada à das cidades brasileiras, apresenta:
A) menor pressão e menor concentração de oxigênio.
B) maior pressão e maior quantidade de oxigênio.
C) maior pressão e maior concentração de gás carbônico.
D) menor pressão e maior temperatura.
E) maior pressão e menor temperatura.
Questão 02. (UFPE) Dois frascos, contendo diferentes gases que não reagem entre si, são interligados através de uma válvula.
Sabe-se que:
• não há variação de temperatura;
• a pressão inicial do gás A é o triplo da pressão inicial do gás B;
• o volume do frasco A é o dobro do frasco B.
Qual será a pressão do sistema (frasco A + B) quando a válvula for aberta?
A) O dobro da pressão do frasco B.
B) 7/3 da pressão do frasco B.
C) 5/3 da pressão do frasco B.
D) 2/3 da pressão do frasco A.
E) 1/3 da pressão do frasco A.
Questão 03 sobre Misturas Gasosas, Efusão e Difusão: (UFBA) Numa sala fechada, foram abertos ao mesmo tempo três frascos que continham, respectivamente, gás amoníaco (NH3), dióxido de enxofre (SO2) e sulfeto de hidrogênio (H2S). Uma pessoa que estava na sala, a igual distância dos três frascos, sentiu o efeito desses gases na seguinte ordem:
A) H2S, NH3 e SO2.
B) H2S, SO2 e NH3.
C) NH3, H2S e SO2.
D) NH3, SO2 e H2S.
E) SO2, NH3 e H2S.
Questão 04. (Mackenzie-SP) Um recipiente com orifício circular contém os gases y e z. A massa molar do gás y é 4,0 e a massa molar do gás z é 36,0. A velocidade de escoamento do gás y será maior em relação à do gás z:
A) 3 vezes.
B) 8 vezes.
C) 9 vezes.
D) 10 vezes.
E) 12 vezes.
Questão 05 sobre Misturas Gasosas, Efusão e Difusão: (Enem–1999) A construção de grandes projetos hidroelétricos também deve ser analisada do ponto de vista do regime das águas e de seu ciclo na região. Em relação ao ciclo da água, pode-se argumentar que a construção de grandes represas:
A) não causa impactos na região, uma vez que a quantidade total de água da Terra permanece constante.
B) não causa impactos na região, uma vez que a água que alimenta a represa prossegue depois rio abaixo com a mesma vazão e velocidade.
C) aumenta a velocidade dos rios, acelerando o ciclo da água na região.
D) aumenta a evaporação na região da represa, acompanhada também por um aumento local da umidade relativa do ar.
E) diminui a quantidade de água disponível para a realização do ciclo da água.
Questão 06. (UFV-MG–2011) A figura a seguir esquematiza três balões de volumes fixos, preenchidos com hélio, argônio e neônio, respectivamente, e ligados por tubos contendo as torneiras T1 e T2, inicialmente fechadas. O volume, a pressão e a temperatura são mostrados ao lado de cada balão. Considere a constante universal dos gases ideais R = 0,082 atm.L.mol-1.K-1.
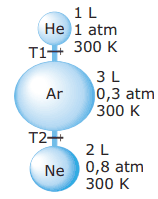
Ao se abrirem as torneiras, mantendo a temperatura constante, as novas pressões, em atm, de He, Ar, Ne e a pressão total serão, respectivamente:
A) 0,167; 0,150; 0,267; 0,584.
B) 0,167; 0,050; 0,130; 0,484.
C) 0,200; 0,150; 0,267; 0,617.
D) 0,200; 0,050; 0,130; 0,350.
Questão 07 sobre Misturas Gasosas, Efusão e Difusão: (PUC-Campinas-SP) A pressão do ar em uma cabine de avião a jato que voa a 10 000 m de altitude equivale à pressão do ar atmosférico a, aproximadamente, 2 400 m de altitude, além de ser mais seco. Considerando tais informações, é possível concluir que a pressão parcial do oxigênio no ar dentro da cabine:
I. é maior do que a pressão parcial que esse gás exerce no ar externo à cabine a 10 000 m de altitude.
II. pode ser calculada pelo emprego da expressão: pressão parcial de O2 = fração em mol de O2 × pressão total do ar.
III. é igual à pressão parcial desse gás no ar a 2 400 m de altitude.
É CORRETO afirmar somente:
A) I.
B) II.
C) III.
D) I e II.
E) II e III.
Questão 08. (UECE) Nas mesmas condições de pressão e temperatura, um gás X atravessa um pequeno orifício a uma velocidade três vezes menor que o hélio. A massa molecular de X é:
A) 30.
B) 32.
C) 36.
D) 40.
E) N.d.a.
Questão 09. (FAAP-SP) Num recipiente fechado, de volume igual a 15 L, está contida uma mistura constituída por 20% molar de CH4 e 80% molar de C2H6, à temperatura de 27 ºC e pressão de 1,64 atm. CALCULE as massas dos componentes da mistura, bem como suas respectivas pressões parciais (massas atômicas: H = 1 u; C = 12 u).
Questão 10 sobre Misturas Gasosas, Efusão e Difusão: De um recipiente escapam 200 mL de oxigênio num certo intervalo de tempo. Pelo mesmo orifício, no mesmo intervalo de tempo, quanto escapa de metano, se a temperatura for a mesma?
Dados: O = 16 u; H = 1 u; C = 12 u

Gabarito com as respostas da melhores Questões de Química sobre Misturas Gasosas, Efusão e Difusão:
01. A;
02. B;
03. C;
04. A;
05. D;
06. A;
07. D;
08. C;
09. m(CH4) = 3,2 g; pCH4 = 0,328 atm
m(C2H6) = 24 g; pC 2H6 = 1,312 atm
10. 283 mL
Doutorando em Genética e Biologia Molecular – UESC-BA
Mestre em Genética e Biologia Molecular – UESC-BA
Pós-Graduado em Metodologia do Ensino de Biologia e Química – FAEL
Licenciado em Ciências Biologias – IFMT/Campus Juína
